题目内容
4.下列各组离子中,能大量共存且加入(或通入)X试剂后发生反应的离子方程式对应正确的是( )| 选项 | 离子组 | 试剂X | 离子方程式 |
| A | Fe3+、Al3+、SiO32-、NO3- | 过量的盐酸 | SiO32-+2H+=H2SiO3↓ |
| B | 透明溶液中:Fe3+、NH4+、SO42-、Cl- | 过量的铜粉 | 2Fe3++Cu=2Fe2++Cu2+ |
| C | Na+、Ba+、HCO3-、Cl- | NaHSO4溶液 | H++HCO3-=CO2↑+H2O |
| D | pH=1的溶液中:Mg2+、Fe2+、NO3-、SO42- | 双氧水 | 2Fe2++H2O2+2H+=2Fe3++2H2O |
| A. | A | B. | B | C. | C | D. | D |
分析 A.Fe3+、Al3+均与SiO32-发生相互促进水解;
B.该组离子之间不反应,加Cu与铁离子发生氧化还原反应;
C.加NaHSO4溶液,生成硫酸钡沉淀;
D.pH=1的溶液,显酸性,离子之间发生氧化还原反应.
解答 解:A.Fe3+、Al3+均与SiO32-发生相互促进水解,不能共存,故A错误;
B.该组离子之间不反应,加Cu与铁离子发生氧化还原反应,离子反应为2Fe3++Cu=2Fe2++Cu2+,故B正确;
C.加NaHSO4溶液,生成硫酸钡沉淀,漏写生成硫酸钡的离子反应,故C错误;
D.pH=1的溶液,显酸性,H+、Fe2+、NO3-发生氧化还原反应,不能共存,故D错误;
故选B.
点评 本题考查离子共存及离子反应,为高频考点,把握习题中的信息、氧化还原反应、水解反应为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.

练习册系列答案
相关题目
14.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 18g2H2O中含有的电子数目为NA | |
| B. | 0.1L0.5mol/LCH3COOH溶液中含有的氢离+数为0.05NA | |
| C. | 常温常压,22.4LC12中含有的分子数为6.02×1023个 | |
| D. | 常温常压下,足量的金属Al与lmolCl2共热,转移电子数为2NA |
15.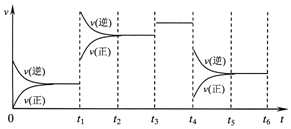 某密闭容器中发生如下反应:X(g)+3Y(g)?2Z(g);△H<0,如图表示该反应的速率(v)随时间(t)变化的关系,t1、t3、t4时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中不正确的是( )
某密闭容器中发生如下反应:X(g)+3Y(g)?2Z(g);△H<0,如图表示该反应的速率(v)随时间(t)变化的关系,t1、t3、t4时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中不正确的是( )
 某密闭容器中发生如下反应:X(g)+3Y(g)?2Z(g);△H<0,如图表示该反应的速率(v)随时间(t)变化的关系,t1、t3、t4时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中不正确的是( )
某密闭容器中发生如下反应:X(g)+3Y(g)?2Z(g);△H<0,如图表示该反应的速率(v)随时间(t)变化的关系,t1、t3、t4时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中不正确的是( )| A. | t1时升高了温度 | B. | t3时加入了催化剂 | ||
| C. | t5~t6时刻,Y转化率最小 | D. | 在t3~t4时间内,X的体积分数最大 |
12.下列化学方程式书写正确的是( )
| A. | 苯酚钠溶液中通入CO2: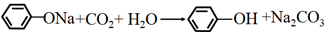 | |
| B. | 常温下CH2=CHCH3与水接触:CH2=CHCH3+H2O→CH3CH(OH)CH3 | |
| C. | 乙醇和金属钠发生反应放出氢气:2CH3CH2OH+2 Na→2CH3CH2ONa+H2↑ | |
| D. | 甲苯与氯气在铁粉催化作用下发生反应: |
19.化学在古代与现代的科技发展中起了十分重要的作用,下列说法中正确的是( )
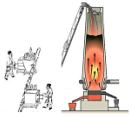 |  |  |  |
| 古代与现代的冶金均运用了相同的化学原理 | 古代与现代的火箭发射均利用了液体燃料 | 古代捣碎中药与现代中药纳米粉碎均是化学变化 | 古代风筝与现代热气球飞行均无需物质直接供给能量 |
| A. | A | B. | B | C. | C | D. | D |
9.25℃时,0.1mol•L-1的HClO2溶液中离子浓度最大的是( )
| A. | H+ | B. | ClO2- | C. | OH- | D. | 无法判断 |
16.下列关于有机化合物的说法正确的是( )
| A. | 乙醇能发生取代反应和加成反应 | |
| B. | 1mol 3-(2-噻吩)丙烯酸(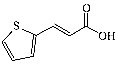 )发生加成反应时最多消耗3mol H2 )发生加成反应时最多消耗3mol H2 | |
| C. | 淀粉和纤维素的分子通式均为(C6H10O5)n,故淀粉和纤维素互为同分异构体 | |
| D. | 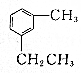 与 与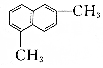 都属于芳香烃,二者互为同系物 都属于芳香烃,二者互为同系物 |
13.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 64gCaC2中含有的共用电子对数为3NA | |
| B. | 标准状况下,11.2L己烷中含有的碳碳键数为2.5NA | |
| C. | 4.6gNO2在标准状况下,含有的分子数为0.1NA | |
| D. | 50mL12 mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA |
14.某太阳能电池的工作原理如图所示.则光照时,失去电子的粒子是( )
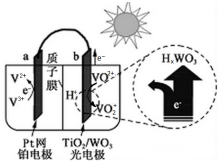

| A. | V2+ | B. | V3+ | C. | VO2+ | D. | VO2+ |