题目内容
在实验室进行下列实验,括号内的实验用品都能用到的是( )
| A、钠的焰色反应(铂丝、氯化钠溶液、稀盐酸) |
| B、蛋白质的盐析(试管、醋酸铅溶液、鸡蛋白溶液) |
| C、硫酸铜晶体里结晶水含量的测定(坩埚、温度计、硫酸铜晶体) |
| D、肥皂的制取(蒸发皿、玻璃棒、甘油) |
考点:化学实验方案的评价
专题:实验评价题
分析:A.稀盐酸洗涤铂丝,灼烧后蘸取氯化钠溶液,再灼烧,观察焰色;
B.醋酸铅溶液为重金属盐;
C.不需要温度计,需要测定加热前后的质量;
D.肥皂的制取,需要油脂和NaOH溶液.
B.醋酸铅溶液为重金属盐;
C.不需要温度计,需要测定加热前后的质量;
D.肥皂的制取,需要油脂和NaOH溶液.
解答:
解:A.稀盐酸洗涤铂丝,灼烧后蘸取氯化钠溶液,再灼烧,观察焰色,则钠的焰色反应实验可完成,故A正确;
B.醋酸铅溶液为重金属盐,可进行蛋白质变性实验,故B错误;
C.不需要温度计,需要测定加热前后的质量,缺少托盘天平,故C错误;
D.肥皂的制取,需要油脂和NaOH溶液,括号内的实验用品不能制取肥皂,故D错误;
故选A.
B.醋酸铅溶液为重金属盐,可进行蛋白质变性实验,故B错误;
C.不需要温度计,需要测定加热前后的质量,缺少托盘天平,故C错误;
D.肥皂的制取,需要油脂和NaOH溶液,括号内的实验用品不能制取肥皂,故D错误;
故选A.
点评:本题考查化学实验方案的评价,为高频考点,涉及焰色反应、蛋白质的性质、结晶水含量测定及肥皂制取等,把握物质的性质及实验基本操作为解答的关键,侧重实验技能的考查,注意操作的可行性、评价性分析,题目难度不大.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
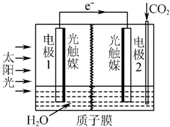 利用人工光合作用合成甲酸的原理为2CO2+2H2O
利用人工光合作用合成甲酸的原理为2CO2+2H2O| 太阳能 |
| 光触媒 |
| A、该装置将太阳能转化为化学能和电能 |
| B、电极1周围pH增大 |
| C、电极2上发生的反应为:CO2+2H++2e-═HCOOH |
| D、H+由电极1室经过质子膜流向电极2室 |
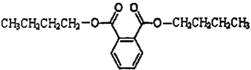 邻苯二甲酸二丁酯是一种常用的塑化剂,其结构简式如图所示.下列关于塑化剂的说法正确的是( )
邻苯二甲酸二丁酯是一种常用的塑化剂,其结构简式如图所示.下列关于塑化剂的说法正确的是( )| A、能溶于水 |
| B、与乙二酸二乙酯互为同系物 |
| C、可用邻苯二甲酸和丁醇酯化制得 |
| D、完全燃烧1mol该有机物需要436.8L O2 |
高铁电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应式为3Zn+2K2FeO4+8H2O═3Zn(OH)2+2Fe(OH)3+4KOH.下列叙述正确的是( )
| A、放电时,负极反应式为3Zn-6e-+6OH-═3Zn(OH)2 |
| B、放电时,正极区溶液的pH减小 |
| C、充电时,每转移3mol电子,阳极有1mol Fe(OH)3被还原 |
| D、充电时,电池的锌电极接电源的正极 |
结合如图装置判断,下列叙述正确的是( )
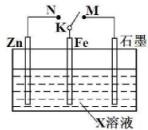

| A、若X为NaCl,K与M相连时,石墨电极反应为2Cl--2e-═Cl2↑ |
| B、若X为硫酸,K与M相连时,Fe作负极受到保护 |
| C、若X为硫酸,K与N相连时,溶液中H+向Fe电极移动 |
| D、若X为NaCl,K与N相连时,溶液中加入少量K3[Fe(CN)6],有蓝色沉淀生成 |
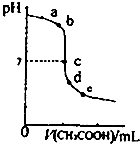 25℃时,向20.00mL NaOH溶液中逐滴加入0.20mo1?L-1的CH3COOH溶液得到如图曲线.下列说法正确的是( )
25℃时,向20.00mL NaOH溶液中逐滴加入0.20mo1?L-1的CH3COOH溶液得到如图曲线.下列说法正确的是( )| A、水电离出的氢离子浓度:a>b |
| B、c点时恰好中和 |
| C、在d~e之间存在如下关系C(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D、e点时溶液中溶质是CH3COONa和CH3COOH |
在塑料原料加工时,添加塑化剂(DCHP)可以使其变得较为柔软,易于加工.塑化剂易溶于有机溶剂,是一种对人体有害的一类物质.塑化剂的一种制备方法如下:
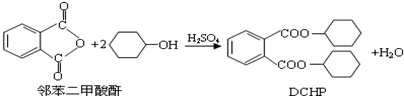
下列说法正确的是( )

下列说法正确的是( )
| A、DCHP的分子式为C20H28O4 |
| B、上述制备DCHP的反应属于取代反应 |
| C、DCHP苯环上的一氯代物有4种 |
| D、1mol DCHP最多可与含4mol NaOH的溶液反应 |

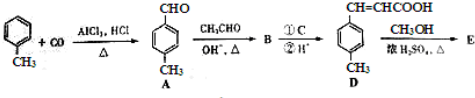
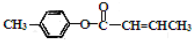 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为