题目内容
水、双氧水都是由H、O元素组成的重要化合物.下列表述正确的是( )
A、H2O2的电子式为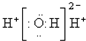 |
| B、4℃时,纯水的pH<7,溶液呈中性 |
| C、H2O2中,质量数之和是质子数之和的两倍 |
| D、273K、101kPa,水分子间的平均距离d(气态)>d(固态)>d(液态) |
考点:电子式、化学式或化学符号及名称的综合,过氧化氢
专题:
分析:A.过氧化氢属于共价化合物,不存在阴阳离子;
B.水的电离是吸热过程,4℃时,水的离子积小于10-14,纯水中氢离子浓度小于10-7;
C.氢原子不含中子数,H2O2的质量数为34,质子数为18;
D.由于冰中的氢键作用,存在四面体结构,水分子的空间利用率不高,分子间距比液态水大.
B.水的电离是吸热过程,4℃时,水的离子积小于10-14,纯水中氢离子浓度小于10-7;
C.氢原子不含中子数,H2O2的质量数为34,质子数为18;
D.由于冰中的氢键作用,存在四面体结构,水分子的空间利用率不高,分子间距比液态水大.
解答:
解:A.过氧化氢属于共价化合物,分子中氧原子之间形成1对共用电子对、氢原子与氧原子之间形成1对共用电子对,电子式为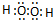 ,故A错误;
,故A错误;
B.纯水呈中性,水的电离是吸热过程,4℃时,水的离子积小于10-14,纯水中氢离子浓度小于10-7,纯水的pH>7,故B错误;
C.H2O2的质量数为34,质子数为18,质量数之和小于质子数之和的两倍,故C错误;
D.由于冰中的氢键作用,存在四面体结构,水分子的空间利用率不高,分子间距比液态水大,水分子间的平均距离:d(气态)>d(固态)>d(液态),故D正确;
故选D.
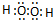 ,故A错误;
,故A错误;B.纯水呈中性,水的电离是吸热过程,4℃时,水的离子积小于10-14,纯水中氢离子浓度小于10-7,纯水的pH>7,故B错误;
C.H2O2的质量数为34,质子数为18,质量数之和小于质子数之和的两倍,故C错误;
D.由于冰中的氢键作用,存在四面体结构,水分子的空间利用率不高,分子间距比液态水大,水分子间的平均距离:d(气态)>d(固态)>d(液态),故D正确;
故选D.
点评:本题考查电子式、水的电离、氢键、物质状态与能量关系等总数,题目难度中等,注意基础知识的理解掌握,注意氢键对水的性物理性质的影响.

练习册系列答案
相关题目
HCN无色有杏仁气味的有毒气体,早期广泛用于船舱、仓库的烟熏灭鼠.已知:HCN( aq)与NaOH(aq)反应的焓变△H=-12.1kJ?mol-1; HCl(aq)与NaOH(aq)反应的焓变△H=-55.6kJ?mol-1.则HCN在水溶液中电离的焓变△H等于( )
| A、-67.7 kJ?mol-1 |
| B、-43.5 kJ?mol-1 |
| C、+43.5 kJ?mol-1 |
| D、+67.7 kJ?mol-1 |
下列化学用语正确的是( )
A、乙酸根离子的结构式: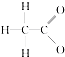 |
| B、乙酸的结构简式C2H4O2 |
| C、3-甲基-1-丁烯的结构简式:(CH3)2CHCH═CH2 |
D、醛基的电子式: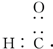 |
在标准状况下,将O2与NO2按1:4的体积比充满一个干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升后,最后烧瓶内溶液的物质的量浓度为( )
| A、0.045mol?L-1 |
| B、0.036mol?L-1 |
| C、0.026mol?L-1 |
| D、0.030mol?L-1 |
下列关于“16g氧气”的叙述中,错误的是( )
| A、物质的量为0.5mol |
| B、气体体积为11.2L |
| C、含有NA 个氧原子 |
| D、含有8 NA个电子 |
对H2O的电离平衡不产生影响的粒子是( )
| A、Na2O2 |
| B、26M3+ |
C、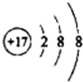 |
D、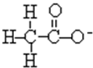 |