题目内容
14.下列元素的原子半径依次减小的是( )| A. | Na、Mg、Al | B. | N、P、As | C. | P、Si、Al | D. | C、Si、P |
分析 同周期自左而右原子半径减小,同主族自上而下原子半径增大,一般电子层越大原子半径越大.
解答 解:A.同周期自左而右原子半径减小,故原子半径Na>Mg>Al,故A正确;
B.同主族自上而下原子半径增大,故原子半径N<P<As,故B错误;
C.同周期自左而右原子半径减小,故原子半径P<Si<Al,故B错误;
D.同周期自左而右原子半径减小,同周期自左而右原子半径减小,一般电子层越大原子半径越大,故原子半径Si>P>C,故D错误.
故选:A.
点评 本题考查原子半径的大小比较,是对元素周期律的应用,从结构上理解微粒半径大小比较,题目主要涉及同主族、同周期比较以及短周期元素比较,注意Cl、Li原子半径.

练习册系列答案
相关题目
5.下列能级的能量大小比较,正确的是( )
| A. | E(4s)>E(3d) | B. | E(6p)>E(5f) | C. | E(6s)<E(5p) | D. | E(4d)<E(5p) |
2.下列化学用语正确的是( )
| A. | CCl4的电子式: | B. | Na2S的形成过程: | ||
| C. | CO2分子的电子式: | D. | 过氧化氢分子的结构式:H-O-O-H |
9.设NA为阿伏加德罗常数,下列说法中正确的是( )
| A. | 标准状况下,11.2L的戊烷所含的分子数为0.5NA | |
| B. | 现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA | |
| C. | 28g乙烯所含共用电子对数目为4NA | |
| D. | 1mol甲基的电子数目为10NA |
19.卤素是最活泼的一族非金属,下列关于卤族元素的说法正确的是( )
| A. | 卤素单质的最外层电子数都是7 | |
| B. | 从上到下,卤素原子的电子层数依次增多,半径依次减小 | |
| C. | 从F到I,原子核对最外层电子的吸引能力依次减弱,原子的得电子能力依次减弱 | |
| D. | 卤素单质与H2化合由易到难顺序为F2<Cl2<Br2<I2 |
6.X、Y、Z、W是四种金属单质,把X浸入Z的硝酸盐溶液中,X的表面有Z析出;X、Y和稀硫酸组成原电池时,X电极上有气泡生成;Z、W相连接后放入稀硫酸中,电子由Z流向W.X、Y、Z三种金属的活动性顺序为( )
| A. | Y>X>Z>W | B. | W>X>Z>Y | C. | X>Y>Z>W | D. | Y>Z>X>W |
3.某化学兴趣小组制备硫化亚铁并探究其自燃性质.
实验I 在石棉网上把研细的硫粉和铁粉按一定比例混合均匀,用灼热的玻璃棒触及混合物,当混合物呈红热状态时,移开玻璃棒,得到黑色FeS.
(1)玻璃棒的作用是加热引发铁与硫发生反应.
(2)常温下,该实验制得的硫化亚铁不能(填“能”或“不能”)自燃.
实验II 将H2S气体长时间通入硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液中进行硫化,制备硫化亚铁.装置示意图如下.
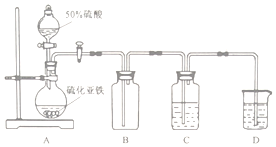
(3)B装置的作用是缓冲瓶(或安全瓶).
(4)C中反应生成硫化亚铁的离子方程式为H2S+Fe2+=FeS↓+2H+
(5)C中的固液混合物经过滤、洗涤、干燥得到产品.检验过滤所得固体物质是否洗涤干净的方法是取少量洗涤液,滴加氯化钡溶液,茗无白色浑浊,则已经洗净.
(6)产品分析结果表:
①表中x=60.50
②总铁质世分数大于亚铁质量分数,原因是产品中含有三价铁杂质
(7)制得的硫化亚铁在常温下能发生缓慢氧化而自燃,写出该过程的化学方程式:4FeS+7O2=2Fe2O3+4SO2(写一个).
实验I 在石棉网上把研细的硫粉和铁粉按一定比例混合均匀,用灼热的玻璃棒触及混合物,当混合物呈红热状态时,移开玻璃棒,得到黑色FeS.
(1)玻璃棒的作用是加热引发铁与硫发生反应.
(2)常温下,该实验制得的硫化亚铁不能(填“能”或“不能”)自燃.
实验II 将H2S气体长时间通入硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液中进行硫化,制备硫化亚铁.装置示意图如下.

(3)B装置的作用是缓冲瓶(或安全瓶).
(4)C中反应生成硫化亚铁的离子方程式为H2S+Fe2+=FeS↓+2H+
(5)C中的固液混合物经过滤、洗涤、干燥得到产品.检验过滤所得固体物质是否洗涤干净的方法是取少量洗涤液,滴加氯化钡溶液,茗无白色浑浊,则已经洗净.
(6)产品分析结果表:
| 硫质量分数/% | 总铁质量分数/% | 亚铁质量分数/% | 硫化亚铁质量分数/% |
| 22.00 | 44.60 | 38.50 | x |
②总铁质世分数大于亚铁质量分数,原因是产品中含有三价铁杂质
(7)制得的硫化亚铁在常温下能发生缓慢氧化而自燃,写出该过程的化学方程式:4FeS+7O2=2Fe2O3+4SO2(写一个).
19.有A、B两种气体,在相同温度、相同压强下,当它们的质量比为2:1时,其体积比为3:2,则A、B的摩尔质量之比为( )
| A. | 1:2 | B. | 2:1 | C. | 2:3 | D. | 4:3 |