题目内容
用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A、24g NaH中阴离子所含电子总数为NA |
| B、1mol苯分子中含有3NA个碳碳单键 |
| C、NO2和H2O反应毎生成2mol HNO3时转移的电子数目为2NA |
| D、在0.1mol/LK2CO3溶液中,阴离子数目大于0.1NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、NaH中阴离子为H-,1molH-中含2mol电子;
B、根据苯的结构来分析;
C、根据NO2和H2O的反应来分析得失电子数;
D、溶液体积不明确.
B、根据苯的结构来分析;
C、根据NO2和H2O的反应来分析得失电子数;
D、溶液体积不明确.
解答:
解:A、NaH中阴离子为H-,1molH-中含2mol电子,24g NaH的物质的量n=
=
=1mol,其中含1moH-,其中含有2mol电子,个数为2NA个,故A错误;
B、苯不是单双键交替结构,苯中的键是介于单双键之间的特殊的键,故B错误;
C、NO2和H2O的反应:3NO2+H2O=2HNO3+NO,此反应转移2mol电子时生成2molHNO3,毎生成2mol HNO3时转移的电子数目为2NA,故C正确;
D、溶液体积不明确,故无法计算溶液中阴离子的数目,故D错误.
故选C.
| m |
| M |
| 24g |
| 24g/mol |
B、苯不是单双键交替结构,苯中的键是介于单双键之间的特殊的键,故B错误;
C、NO2和H2O的反应:3NO2+H2O=2HNO3+NO,此反应转移2mol电子时生成2molHNO3,毎生成2mol HNO3时转移的电子数目为2NA,故C正确;
D、溶液体积不明确,故无法计算溶液中阴离子的数目,故D错误.
故选C.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 综合自测系列答案
综合自测系列答案
相关题目
在下列有FeCl3溶液参加的反应中,与Fe3+发生氧化还原反应的是( )
①FeCl3与Cu反应
②FeCl3与H2S反应
③FeCl3与KI反应
④FeCl3滴入沸水中
⑤FeCl3与NaHCO3反应
⑥FeCl3溶液中滴入石蕊试液.
①FeCl3与Cu反应
②FeCl3与H2S反应
③FeCl3与KI反应
④FeCl3滴入沸水中
⑤FeCl3与NaHCO3反应
⑥FeCl3溶液中滴入石蕊试液.
| A、③④⑤⑥ | B、③④⑤ |
| C、④⑤⑥ | D、①②③ |
下列各图所示装置属于原电池的是( )
A、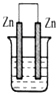 NaCl溶液 |
B、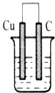 HCl溶液 |
C、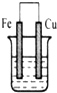 CuSO4溶液 |
D、 蔗糖溶液 |
微粒有多种表示方式,下列各组不同表示方式一定代表同种微粒的是( )
| A、C3H6、CH2═CHCH3 |
B、-OH、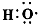 |
C、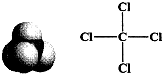 |
D、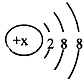 、S2- 、S2- |
去年年末,今年年初我国多省市遭遇雾霾笼罩,“PM2.5”数据监测纳入公众视野.“PM2.5”是指大气中直径小于或等于2.5微米的细小颗粒物,也称为可入肺颗粒物.下列有关说法中,错误的是( )
| A、雾霾有可能产生丁达尔现象 |
| B、城市由于汽车尾气的大量排放,比农村形成雾霾天气的可能性更大 |
| C、氟利昂作制冷剂会加剧雾霾天气的形成 |
| D、雾霾天气严重危害人体健康 |
化学与生产、生活、社会密切相关.下列有关说法错误的是( )
| A、明矾和氯气均可用于水的消毒、杀菌 |
| B、地沟油不能食用,但可以在循环经济中发挥作用 |
| C、硬铝属于合金材料,餐桌上的瓷盘属于硅酸盐制品 |
| D、不需要通过化学反应就能从海水中获得食盐和淡水 |
下列表示对应化学反应的离子方程式正确的是( )
| A、NH4HSO4溶液中加入足量的Ba(OH)2溶液:OH-+H++Ba2++SO4-2=BaSO4↓+H2O |
| B、小苏打溶液中加入足量的Ca(OH)2溶液:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| C、用稀硝酸洗涤试管内壁银镜:Ag+2H++NO3-=Ag++NO↑+H2O |
| D、向Mg(OH)2悬浊液中滴加FeCl3溶液,生成红褐色沉淀:3OH-+Fe3+=Fe(OH)3↓ |
下列说法正确的是( )
| A、已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c (Mg2+)?c (CO32-)=6.82×10-6 |
| B、常温下,在0.10 mol?L-1的NH3?H2O溶液中加入少量NH4Cl晶体,c( NH4+)/c(NH3?H2O)值变大 |
| C、pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c (H2CO3) |
D、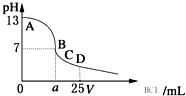 室温下,在25 mL 0.1 mol?L-1NaOH溶液中逐滴加入0.2 mol?L-1HCl溶液,pH与滴加HCl溶液体积的关系曲线如图所示. 室温下,在25 mL 0.1 mol?L-1NaOH溶液中逐滴加入0.2 mol?L-1HCl溶液,pH与滴加HCl溶液体积的关系曲线如图所示. |
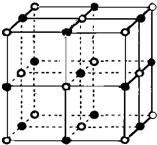 决定物质性质的重要因素是物质结构.请回答下列问题.
决定物质性质的重要因素是物质结构.请回答下列问题.