题目内容
14.下列各组比较中,前者大于后者的是( )| A. | 等质量的硫磺和硫蒸气分别完全燃烧放出的热量 | |
| B. | 中和体积与pH都相等的醋酸溶液和盐酸所消耗的NaOH的物质的量 | |
| C. | 2H2(g)+O2(g)═2H2O(l)△H1 2H2(g)+O2(g)═2H2O(g)△H2,两个反应热△H的大小 | |
| D. | 相同温度、相同浓度的NH4Cl和NH4HSO4溶液中c(NH4+) |
分析 A.硫蒸气变化为硫固体为放热过程;
B.醋酸为弱电解质,溶液中部分电离出氢离子,所以分别中和pH与体积均相同的盐酸和醋酸,醋酸消耗氢氧化钠的质量多;
C.物质的燃烧是放热的过程,液态水变为气态水需要吸收热量,△H<0为放热;
D.NH4Cl中,铵根离子正常水解,而NH4HSO4溶液中H+抑制铵根离子水解.
解答 解:A.硫蒸气变化为硫固体为放热过程,则等量的硫蒸气和硫固体在氧气中分别完全燃烧,放出热量硫蒸气多,前者小于后者,故A错误;
B.醋酸为弱电解质,溶液中部分电离出氢离子,所以分别中和pH与体积均相同的醋酸和盐酸,醋酸消耗氢氧化钠的质量多,前者大于后者,故B正确;
C.物质的聚集状态不同,放出的热量不同,水蒸气液化时放热,生成H2O(g)放出的热量少,由于氢气的燃烧为放热反应,△H<0,则有|△H1|>|△H2|,则△H1<△H2,故C错误;
D.相同温度、相同浓度的NH4Cl中,铵根离子正常水解,NH4HSO4溶液中H+抑制铵根离子水解,故NH4HSO4溶液中c(NH4+)大于NH4Cl溶液中的c(NH4+),故D错误;
故选B.
点评 本题考查了反应热量变化,弱电解质的电离平衡,盐类水解,反应热的大小比较等,掌握基础是关键,题目难度中等.

练习册系列答案
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
4.实验室有一瓶氮肥样品,可能含有NH4HC03、NH4Cl和NH4N03中的一种或多种.通过下列实验鉴别成分:称量样品23.90g,加人100mL2.0mol•L-1盐酸充分反应后溶液呈酸性,且放出的气体在标准状况下为2.24L,再向上述反应过后的溶液中加入足量AgN03溶液至不再产生沉淀,所得沉淀为28.7g.根据上述实验事实得出的结论正确的是( )
| A. | 该样品中一定含有NH4HC03和NH4Cl | |
| B. | 该样品中含N元素的质量分数为17.57% | |
| C. | 该样品若和足量烧碱反应,将消耗0.4mol NaOH | |
| D. | 根据上述数据可以确定原样品中含有5.3g NH4N03 |
2.X、Y、Z、R是短周期主族元素,X原子最外层电子数是次外层的两倍,Y元素在地壳中的含量最多,Z元素的化合物的焰色反应呈黄色,R原子的核外电子数是X原子与Z原子的核外电子数之和.下列叙述正确的是( )
| A. | 原子半径的大小顺序:r(X)>r(Y)>r(Z)>r(R) | |
| B. | 含有Y、Z、R三种元素的化合物最多只有2种 | |
| C. | 元素R和Y形成的化合物RY2是一种高效安全灭菌消毒剂 | |
| D. | Y与Z形成的两种化合物中的化学键和晶体类型均相同 |
9.1.52g铜镁合金完全溶解于50mL密度为1.40g•mL-1、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体 1 120mL(标准状况),向反应后的溶液中加入1.0mol•L-1NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是( )
| A. | 该合金中铜与镁的物质的量之比是1:2 | |
| B. | 该浓硝酸中HNO3的物质的量浓度是14.0 mol•L-1 | |
| C. | NO2和N2O4的混合气体中,NO2的体积分数是80% | |
| D. | 得到2.54 g沉淀时,加入NaOH溶液的体积是640 mL |
19.下列现象或新技术的应用中,不涉及胶体性质的是( )
| A. | 肾功能衰竭等疾病,可利用血液透析进行治疗 | |
| B. | 在饱和氯化铁溶液中滴加NaOH溶液,产生红褐色沉淀 | |
| C. | 清晨,在茂密的树林中,可看到枝叶间透过的一道光线 | |
| D. | 使用微波手术刀进行外科手术,可使开刀处的血液迅速凝固而减少失血 |
6.用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 78gNa2O2固体中所含离子总数为4NA | |
| B. | 常温常压下,14gN2与CO组成的混合气体含有的原子数为NA | |
| C. | 1molCl2完全反应则转移电子数一定为2NA | |
| D. | Na2O2与水反应产生22.4LO2,则转移电子数为2 NA |
4.下列除杂试剂、主要操作或方法均正确的是(括号内为杂质)( )
| 选项 | 原物质及杂质 | 除杂试剂 | 主要操作或方法 |
| A | 乙酸乙酯(乙酸) | Na2CO3 | 过滤 |
| B | Na2CO3(s )[NaHCO3(s )] | NaOH溶液 | 转化法 |
| C | FeCl2(CuCl2) | Zn | 过滤 |
| D | 苯(溴) | NaOH溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
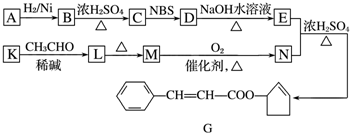
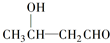
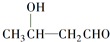 $\stackrel{△}{→}$CH3CH═CHCHO+H2O
$\stackrel{△}{→}$CH3CH═CHCHO+H2O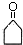 ,G中官能团的名称为碳碳双键和酯基.
,G中官能团的名称为碳碳双键和酯基. ,反应类型加成反应.
,反应类型加成反应.