题目内容
19.某链状有机物分子中含x个-CH3,y个-CH2-,z个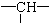 ,其余为氯原子.则氯原子的个数为( )
,其余为氯原子.则氯原子的个数为( )| A. | 2y+3x-x | B. | z+2-x | C. | 2y+z-x | D. | z+2y+2-x |
分析 某链状有机物分子中含x个-CH3,y个-CH2-,z个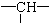 ,其余为氯原子,该有机物为卤代烃,饱和烷烃的通式CnH2n+2,在含x个-CH3,y个-CH2-,z个
,其余为氯原子,该有机物为卤代烃,饱和烷烃的通式CnH2n+2,在含x个-CH3,y个-CH2-,z个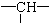 的有机物中,碳原子个数为:x+y+z,所以氢原子数目是:2(x+y+z)+2,即2x+2y+2z+2个,含有H原子数为:3x+2y+z,氯原子补充H原子数,则一定满足:2x+2y+2z+2=3x+2y+z+N(Cl),据此计算出氯原子数目即可.
的有机物中,碳原子个数为:x+y+z,所以氢原子数目是:2(x+y+z)+2,即2x+2y+2z+2个,含有H原子数为:3x+2y+z,氯原子补充H原子数,则一定满足:2x+2y+2z+2=3x+2y+z+N(Cl),据此计算出氯原子数目即可.
解答 解:某链状有机物分子中含x个-CH3,y个-CH2-,z个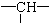 ,其余为氯原子,该有机物为卤代烃,
,其余为氯原子,该有机物为卤代烃,
饱和烷烃的通式CnH2n+2,在含x个-CH3,y个-CH2-,z个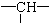 的有机物中,碳原子个数为:x+y+z,所以氢原子数目是:2(x+y+z)+2,即2x+2y+2z+2个,含有H原子数为:3x+2y+z,
的有机物中,碳原子个数为:x+y+z,所以氢原子数目是:2(x+y+z)+2,即2x+2y+2z+2个,含有H原子数为:3x+2y+z,
氯原子为取代H原子形成的,则一定满足:2x+2y+2z+2=3x+2y+z+N(Cl),
解得:N(Cl)=z+2-x,
故选B.
点评 本题考查有机化合物中成键特征,题目难度不大,明确常见有机物组成、结构特点为解答关键,试题侧重基础知识的考查,培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
10.下列离子方程式中,正确的是( )
| A. | Ca(ClO)2溶液中通入过量的CO2:Ca2++2ClO-+CO2+H2O=CaCO3↓+2HClO | |
| B. | 钠和冷水反应:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 氯气和水反应:Cl2+H2O=2H++Cl-+ClO- | |
| D. | NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO32-+H2O |
14.在水溶液中能量共存的一组离子是( )
| A. | Na+、Ba2+、Cl-、NO3- | B. | Pb2 +、Hg2 +、S2 -、SO42 - | ||
| C. | NH4+、H+、S2O32-、PO43- | D. | ClO-、Al3 +、Br-、CO32 - |
4.以下实验能获得成功的是( )
| A. | 用溴水鉴别甲苯、己烷、己烯 | |
| B. | 将稀硫酸、稀硝酸和苯混合加热制硝基苯 | |
| C. | 苯和硝基苯混合物采用分液的方法分离 | |
| D. | 用CuSO4溶液除去由电石和水反应生成的乙炔气体中的杂质 |
11.短周期元素X、Y、Z、W,它们的原子序数依次增大.X与Z同主族,并且原子序数之和为20.Y原子的质子数为Z原子的质子数的一半,W原子的最外层电子数比Y原子的最外层电子数多2个.下列叙述正确的是( )
| A. | 原子半径Z>W>Y>X | |
| B. | Y的最高价氧化物对应的水化物可与其气态氢化物发生化合反应 | |
| C. | 气态氢化物的稳定性Z>W | |
| D. | X与Y的最高正化合价之和的数值等于10 |
8.下列各组物质中,属于同素异形体的是( )
| A. | S2、S4 | B. | 碘晶体、碘蒸气 | ||
| C. | H、D | D. | ${\;}_{8}^{16}$O2、${\;}_{8}^{18}$O2 |
9.稀土是一种不可再生的战略性资源,被广泛应用于电子信息、国防军工等多个领域.一种从废弃阴极射线管(CRT)荧光粉中提取稀土元素钇(Y)的工艺流程如图1:
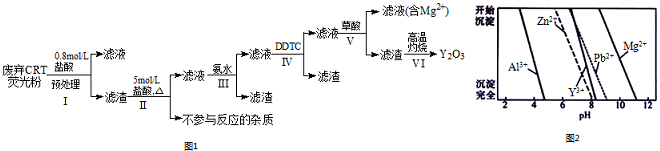
已知:①废弃CRT荧光粉的化学组成(某些不参与反应的杂质未列出)如下表所示;
②不同离子沉淀的pH如图2所示.
(1)步骤I中进行原料预处理的目的为除去ZnO和Al2O3;富集稀土元素;降低后续耗酸量等.(答两点)
(2)步骤Ⅱ中有黄绿色气体产生,该反应的化学方程式为PbO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$PbCl2+Cl2↑+2H2O.
(3)步骤Ⅲ中发生的主要反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
(4)步骤Ⅳ中除杂试剂DDTC除去的杂质离子有Zn2+、Pb2+,其不能通过直接加碱的方法除去,原因为Zn2+、Pb2+与Y3+沉淀的pH相近,三者因同时沉淀而无法分离.
(5)步骤V中Y3+沉淀完全时,需保证滴加草酸后的溶液中c(C2O42-)不低于2.0×10-6mol/L.
(已知:当离子浓度小于10-5mol/L时,沉淀就达完全;Ksp[Y2(C2O4)3]=8.0×10-28)
(6)步骤Ⅵ中草酸钇隔绝空气加热可以得到Y2O3,该反应的化学方程式为Y2(C2O4)3$\frac{\underline{\;\;△\;\;}}{\;}$Y2O3+3CO↑+3CO2↑.

已知:①废弃CRT荧光粉的化学组成(某些不参与反应的杂质未列出)如下表所示;
| 阶段/含量%/成分 | Y2O3 | ZnO | Al2O3 | PbO2 | MgO |
| 预处理前 | 24.28 | 41.82 | 7.81 | 1.67 | 0.19 |
| 预处理后 | 68.51 | 5.42 | 4.33 | 5.43 | 0.50 |
(1)步骤I中进行原料预处理的目的为除去ZnO和Al2O3;富集稀土元素;降低后续耗酸量等.(答两点)
(2)步骤Ⅱ中有黄绿色气体产生,该反应的化学方程式为PbO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$PbCl2+Cl2↑+2H2O.
(3)步骤Ⅲ中发生的主要反应的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
(4)步骤Ⅳ中除杂试剂DDTC除去的杂质离子有Zn2+、Pb2+,其不能通过直接加碱的方法除去,原因为Zn2+、Pb2+与Y3+沉淀的pH相近,三者因同时沉淀而无法分离.
(5)步骤V中Y3+沉淀完全时,需保证滴加草酸后的溶液中c(C2O42-)不低于2.0×10-6mol/L.
(已知:当离子浓度小于10-5mol/L时,沉淀就达完全;Ksp[Y2(C2O4)3]=8.0×10-28)
(6)步骤Ⅵ中草酸钇隔绝空气加热可以得到Y2O3,该反应的化学方程式为Y2(C2O4)3$\frac{\underline{\;\;△\;\;}}{\;}$Y2O3+3CO↑+3CO2↑.
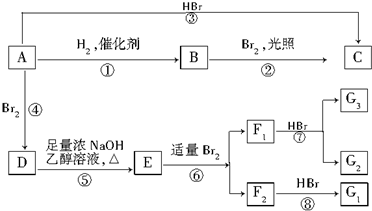
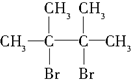 )(F1和F2互为同分异构体)(G1和G2互为同分异构体)
)(F1和F2互为同分异构体)(G1和G2互为同分异构体) .
.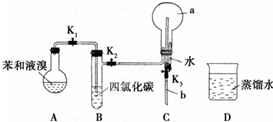
 ,烧瓶a中的实验现象是烧杯中的水沿玻璃管上升进入烧瓶,形成喷泉.
,烧瓶a中的实验现象是烧杯中的水沿玻璃管上升进入烧瓶,形成喷泉.