题目内容
将一定量铁粉投入到2L 0.5mol/L稀硫酸中,充分反应后,铁完全溶解,产生的气体在标准状况下的体积约为3.36L,求:
(1)消耗的铁粉的质量.
(2)向反应后的混合液中加入1mol/L NaOH溶液,会消耗掉NaOH溶液的体积为多少?
(要求:1、用物质的量进行计算.2、写出计算步骤.)
(1)消耗的铁粉的质量.
(2)向反应后的混合液中加入1mol/L NaOH溶液,会消耗掉NaOH溶液的体积为多少?
(要求:1、用物质的量进行计算.2、写出计算步骤.)
考点:化学方程式的有关计算
专题:计算题
分析:(1)发生反应:Fe+H2SO4(稀)=FeSO4+H2↑,根据n=
计算氢气的物质的量,根据方程式计算消耗Fe的物质的量,再根据m=nM计算消耗Fe的质量;
(2)向反应后溶液中加入氢氧化钠溶液,硫酸、硫酸亚铁都与氢氧化钠反应,最终溶液中溶质为Na2SO4,根据钠离子、硫酸根守恒:n(NaOH)=2n(Na2SO4)=2n(H2SO4),再根据V=
计算氢氧化钠溶液的体积.
| V |
| Vm |
(2)向反应后溶液中加入氢氧化钠溶液,硫酸、硫酸亚铁都与氢氧化钠反应,最终溶液中溶质为Na2SO4,根据钠离子、硫酸根守恒:n(NaOH)=2n(Na2SO4)=2n(H2SO4),再根据V=
| n |
| c |
解答:
解:(1)标况下,3.36L氢气的物质的量=
=0.15mol,
Fe+H2SO4(稀)=FeSO4+H2↑
1 1
n(Fe) 0.15mol
n(Fe)=
=0.15mol,
故m(Fe)=0.15mol×56g/mol=8.4g,
答:消耗铁的质量为8.4g.
(2)向反应后溶液中加入氢氧化钠溶液,硫酸、硫酸亚铁都与氢氧化钠反应,最终溶液中溶质为Na2SO4,根据钠离子、硫酸根守恒:n(NaOH)=2n(Na2SO4)=2n(H2SO4)=2×2L×0.5mol/L=2mol,故需要氢氧化钠溶液的体积=
=2L,
答:需要氢氧化钠溶液的体积为2L.
| 3.36L |
| 22.4L/mol |
Fe+H2SO4(稀)=FeSO4+H2↑
1 1
n(Fe) 0.15mol
n(Fe)=
| 0.15mol×1 |
| 1 |
故m(Fe)=0.15mol×56g/mol=8.4g,
答:消耗铁的质量为8.4g.
(2)向反应后溶液中加入氢氧化钠溶液,硫酸、硫酸亚铁都与氢氧化钠反应,最终溶液中溶质为Na2SO4,根据钠离子、硫酸根守恒:n(NaOH)=2n(Na2SO4)=2n(H2SO4)=2×2L×0.5mol/L=2mol,故需要氢氧化钠溶液的体积=
| 2mol |
| 1mol/L |
答:需要氢氧化钠溶液的体积为2L.
点评:本题考查化学方程式的计算,难度中等,(2)中注意利用守恒法计算,简化计算步骤,侧重对学生分析思维能力的考查.

练习册系列答案
相关题目
当2NO2(g)?N2O4(g)反应达平衡后,保持其它条件不变,压缩混合气体体积,所观察到的现象是( )
| A、红棕色先变浅后变深最终颜色较浅 |
| B、红棕色先变浅后变深最终颜色较深 |
| C、红棕色先变深后再变浅最终颜色较浅 |
| D、红棕色先变深后变浅最终颜色较深 |
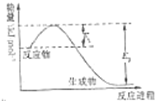 氮是地球上含量丰富的一种元素,氮及其化合物在生产生活中有着重要作用.请回答下列问题:
氮是地球上含量丰富的一种元素,氮及其化合物在生产生活中有着重要作用.请回答下列问题: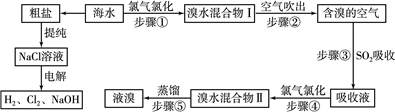

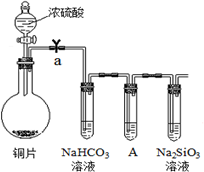 下表是元素周期表的一部分,表中所列字母分别代表一种元素.
下表是元素周期表的一部分,表中所列字母分别代表一种元素.