题目内容
18.已知短周期元素的离子,aA2+、bB+、cC2-、dD-具有相同的电子层结构,则( )| A. | 原子半径:A>B>C>D | B. | 原子序数:d>c>b>a | ||
| C. | 离子半径:C2->D->B+>A2+ | D. | 单质的还原性:A>B>D>C |
分析 短周期元素的离子aA2+、bB+、cC2-、dD-具有相同电子层结构,核外电子数相等,所以a-2=b-1=c+2=d+1,C、D为非金属,应处于第二周期,故C为O元素,D为F元素,A、B为金属应处于第三周期,A为Mg元素,B为Na元素,结合元素周期律解答.
解答 解:短周期元素的离子aA2+、bB+、cC2-、dD-具有相同电子层结构,核外电子数相等,所以a-2=b-1=c+2=d+1,C、D为非金属,应处于第二周期,故C为O元素,D为F元素,A、B为金属应处于第三周期,A为Mg元素,B为Na元素,
A.根据元素在周期表中的位置可知原子半径Na>Mg>O>F,故A错误;
B.由以上分析可知a=12,b=11,c=8,d=9,则由a>b>d>c,故B错误;
C.具有相同核外电子排布的离子,核电荷数越大,则半径越小,则离子半径:C2->D->B+>A2+,故C正确;
D.元素的金属性越强,则失电子能力越强,同周期元素从左到右元素的金属性逐渐减弱,则还原性:B>A>C>D,故D错误.
故选C.
点评 本题考查原子结构和周期律的综合应用,为高频考点,把握元素的性质、元素周期律、元素的推断等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
8.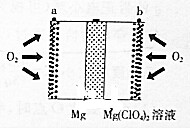 镁空气电池具有比锂电池更好的安全性和更低的成本,主要用于备用电源、军事应用,其工作原理如图所示.下列说法错误的是( )
镁空气电池具有比锂电池更好的安全性和更低的成本,主要用于备用电源、军事应用,其工作原理如图所示.下列说法错误的是( )
 镁空气电池具有比锂电池更好的安全性和更低的成本,主要用于备用电源、军事应用,其工作原理如图所示.下列说法错误的是( )
镁空气电池具有比锂电池更好的安全性和更低的成本,主要用于备用电源、军事应用,其工作原理如图所示.下列说法错误的是( )| A. | 放电时Mg在负极被ClO4-氧化 | |
| B. | 正极的电极反应为:O2+2H2O+4e-═4OH- | |
| C. | 电池总反应为2Mg+O2+2H2O═2Mg(OH)2 | |
| D. | 理论上外电路流过1mol电子时电池总质量增加8.0g |
6.下列工业废气经过处理后可作为燃料的是( )
| A. | 高炉煤气 | B. | 硫酸工业废气 | C. | 炼油厂气 | D. | 硝酸工业废气 |
13.下列关于元素周期表的叙述正确的是( )
| A. | 元素周期表中有18列,即18个族 | |
| B. | 目前使用的元素周期表中,最长的周期含有32种元素 | |
| C. | 短周期元素是指1~20号元素 | |
| D. | 原子的种类和元素的种类一样多 |
10.下列各组给定原子序数的元素,不能形成原子个数之比为1:1共价化合物的是( )
| A. | 3和17 | B. | 1和8 | C. | 6和8 | D. | 1和9 |
7.3.2g铜与过量的硝酸(8mol•L-1,60mL)充分反应后,硝酸的还原产物有NO、NO2,反应后溶液中所含H+离子为nmol.此时溶液中所含NO3-的物质的量为( )
| A. | 0.28mol | B. | 0.3lmol | C. | (n+0.2)mol | D. | (n+0.1)mol |
8.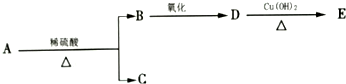 分子式为C9H18O2的有机物A有下列转化关系:其中B、C的相对分子质量相等,则A的可能的结构简式有( )
分子式为C9H18O2的有机物A有下列转化关系:其中B、C的相对分子质量相等,则A的可能的结构简式有( )
 分子式为C9H18O2的有机物A有下列转化关系:其中B、C的相对分子质量相等,则A的可能的结构简式有( )
分子式为C9H18O2的有机物A有下列转化关系:其中B、C的相对分子质量相等,则A的可能的结构简式有( )| A. | 7种 | B. | 8种 | C. | 9种 | D. | 10种 |

 .
.