题目内容
13.稀土元素是周期表中ⅢB族钪、钇和镧系元素之总称,金属活泼性仅次于碱金属和碱土金属元素,它们的性质极为相似,常见化合价为+3价.其中钇(Y)元素是激光和超导的重要材料.我国蕴藏着丰富的含钇矿石(Y2FeBe2Si2O10),工业上通过如下生产流程可获得氧化钇.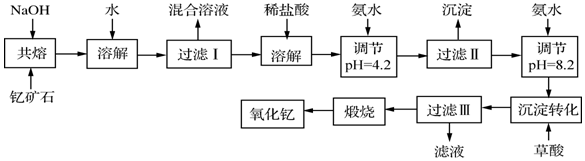
已知:
①有关金属离子形成氢氧化物沉淀时的pH见下表.
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe3+ | 2.7 | 3.7 |
| Y3+ | 6.0 | 8.2 |
请回答下列问题:
(1)若改用氧化物的形式表示Y2FeBe2Si2O10组成,则化学式为Y2O3•FeO•2BeO•2SiO2
(2)过滤Ⅲ所得滤液的溶质主要有NH4Cl、(NH4)2C2O4(填化学式)
(3)①欲从过滤I所得混合溶液中制得Be(OH)2沉淀,最好选用bd两种试剂,再通过必要的操作即可实现.
a.NaOH溶液 b.氨水 c.CO2 d.盐酸
②写出Na2BeO2与足量盐酸发生反应的离子方程式BeO22-+4H+=Be2++2H2O.
(4)能否用氨水直接将溶液的pH调节至8.2,不能(填能或不能),(若不能,请说明理由)第一步用氨水是为了使Fe3+转化为沉淀而除去.
(5)写出沉淀转化步骤中沉淀转化的化学方程式2Y(OH)3+3H2C2O4═Y2(C2O4)3+6H2O.
分析 钇矿石与氢氧化钠共熔,加水溶解后可生成Na2SiO3、Na2BeO2,以及Y(OH)3和Fe2O3沉淀,过滤后加入盐酸溶解,在此基础上加入氨水,由表中数据可知首先生成Fe(OH)3沉淀,加入草酸可生成Y2(C2O4)3,煅烧可生成Y2O3,
(1)依据元素化合价和原子守恒书写元素的氧化物组成;
(2)根据沉淀转化步骤可知过滤Ⅲ所得滤液的溶质;
(3)①周期表中,铍、铝元素处于第二周期和第三周期的对角线位置,化学性质相似,欲从Na2SiO3和Na2BeO2的混合溶液中制得Be(OH)2沉淀,所以Na2BeO2的性质和NaAlO2类比推断;加过量的盐酸,硅酸钠反应生成硅酸沉淀,Na2BeO2的反应生成氯化铍溶液,再加入过量氨水沉淀铍离子;
②Na2BeO2与足量盐酸反应生成氯化铍和氯化钠溶液;
(4)依据图表中的PH数据分析判断三价铁离子完全沉淀,钇离子不沉淀的溶液PH为3.7-6.0;继续加氨水调节pH=8.2是把钇离子全部沉淀的反应;
(5)根据Y2(C2O4)3比Y(OH)3更难溶可写出沉淀转化的化学方程式.
解答 解:(1)钇矿石(Y2FeBe2Si2O10)的组成用氧化物的形式可表示为:Y2O3•FeO•2BeO•2SiO2,故答案为:Y2O3•FeO•2BeO•2SiO2;
(2)在过滤Ⅱ的滤液(含有YCl3)里加氨水后又加草酸,故过滤Ⅲ所得滤液的溶质为NH4Cl、(NH4)2C2O4,故答案为:NH4Cl、(NH4)2C2O4;
(3)①周期表中,铍、铝元素处于第二周期和第三周期的对角线位置,化学性质相似,欲从Na2SiO3和Na2BeO2的混合溶液中制得Be(OH)2沉淀,所以Na2BeO2的性质和NaAlO2类比推断;加过量的盐酸,硅酸钠反应生成硅酸沉淀,Na2BeO2的反应生成氯化铍溶液,再加入过量氨水沉淀铍离子,故答案为:bd;
②Na2BeO2与足量盐酸发生反应生成氯化铍氯化钠和水,反应的离子方程式为:BeO22-+4H+=Be2++2H2O,故答案为:BeO22-+4H+=Be2++2H2O;
(4)三价铁离子开始沉淀到沉淀完全的PH范围为:2.7-3.7;钇离子开始沉淀和沉淀完全的PH为:6.0-8.2;所以使Fe3+沉淀完全,须用氨水调节pH为3.7至6.0;继续加氨水调节pH=8.2是把钇离子全部沉淀的反应,故答案为:不能,第一步用氨水是为了使Fe3+ 转化为沉淀而除去;
(5)加草酸将Y(OH)3转化为Y2(C2O4)3的化学方程式:2Y(OH)3+3H2C2O4═Y2(C2O4)3+6H2O,故答案为:2Y(OH)3+3H2C2O4═Y2(C2O4)3+6H2O.
点评 本题考查了工艺流程图,为高频考点,侧重于学生的分析能力和实验能力的考查,注重试剂的选择,化学方程式的配平等,难度较大.

 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案| A. | 2H2(g)+O2(g)═2H2O(g)△H1 2H2(g)+O2(g)═2H2O(l)△H2 | |
| B. | S(g)+O2(g)═SO2(g)△H1 S(s)+O2(g)═SO2(g)△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)═CO(g)△H1 C(s)+O2(g)═CO2(g)△H2 | |
| D. | 2HCl(g)═H2(g)+Cl2(g)△H1 H2(g)+Cl2(g)═2HCl(g)△H2 |
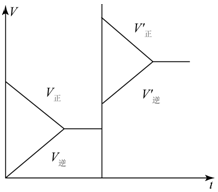 对于达平衡的可逆反应X+Y?W+Z,增大压强则正、逆反应速度(v)的变化如图,分析可知X、Y、Z,W的聚集状态可能是( )
对于达平衡的可逆反应X+Y?W+Z,增大压强则正、逆反应速度(v)的变化如图,分析可知X、Y、Z,W的聚集状态可能是( )| A. | Z、W为气体,X、Y中之一为气体 | B. | X、Y中之一为气体,Z、W为非气体 | ||
| C. | X、Y、Z、W皆为气体 | D. | X、Y为气体,Z、W中之一为气体 |
【实验I】制备NaNO2
该小组查阅资料知:2NO+Na2O2=2NaNO2;2NO2+Na2O2═2NaNO3
设计制备装置如下(夹持装置略去):
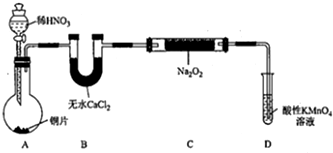
(1)装置D可将剩余的NO氧化成NO3-,发生反应的离子方程式为5NO+3MnO4-+4H+=5NO3-+3Mn2++2H2O.
(2)如果没有B装置,C中发生的副反应有2Na2O2+2H2O=4NaOH+O2↑、2NO+O2=2NO2.
(3)甲同学检查完装置气密性良好后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质.于是在A、B装置增加了在A、B之间增加装有水的洗气瓶装置,改进后提高了NaNO2的纯度.
【实验Ⅱ】测定制取的样品中NaNO2的含量
步骤:
a.在5个有编号的带刻度试管(比色管)中分别加入不同量的NaNO2溶液,各加入1mL的M溶液(M遇NaNO2呈紫红色,NaNO2浓度越大颜色越深),再加蒸馏水至总体积均为10mL并振荡,制成标准色阶:
| 试管编号 | ① | ② | ③ | ④ | ⑤ |
| NaNO2含量/mg•L-1 | 0 | 20 | 40 | 60 | 80 |
(4)步骤b中比较结果是:待测液颜色与③号色阶相同,则甲同学制得的样品中NaNO2的质量分数是40%.
(5)用目视比色法证明维生素C可以有效降低NaNO2的含量.设计并完成下列实验报告.
| 实验方案 | 实验现象 | 实验结论 |
| 取5ml待测液加入维生素C,振荡,再加入1mlM溶液,加入至蒸馏水10mL,再振荡,与③好色阶对比 | 紫红色比③色阶浅 | 维生素C可以有效降低NaNO2的含量 |
| A. | $\frac{84{w}_{2}-53{w}_{1}}{31{w}_{1}}$ | B. | $\frac{84{w}_{2}-53{w}_{1}}{31{w}_{1}}$ | ||
| C. | $\frac{84{w}_{2}-53{w}_{1}}{31{w}_{1}}$ | D. | $\frac{115{w}_{2}-84{w}_{1}}{31{w}_{1}}$ |
| A. | 6.4g | B. | 4.8g | C. | 17.6g | D. | 20.2g |
| A. | 用干净的铂丝蘸取少量溶液在酒精灯外焰上灼烧,发现火焰呈黄色,则溶液中无K+ | |
| B. | 检验某补铁药片(主要成分为亚铁化合物)是否氧化变质,使用氯水和硫氰化钾溶液 | |
| C. | 向某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32- | |
| D. | 向某溶液X中滴加盐酸无明显现象,再滴加BaCl2溶液有白色沉淀,则X中含有SO42- |
| A. | 次氯酸钠溶液可用作环境的杀菌消毒 | |
| B. | 硅胶可用作商品包装袋的干燥剂 | |
| C. | 爆竹燃放后,硫燃烧生成SO3 | |
| D. | 施肥时,草木灰不能与胺态氮肥混合使用 |
