题目内容
12.下列实验描述正确的是( )| A. | 向淀粉水解后的溶液中加入碘水,溶液变蓝色,证明淀粉没有水解 | |
| B. | 向NaOH溶液中滴加浓度均为0.1mol•L-1的FeCl3和AlCl3混合溶液,出现红褐色沉淀,由此可知Ksp[Fe(OH)3]<Ksp[Al(OH)3] | |
| C. | 向待测试样中加入过量稀盐酸无现象,再滴加BaCl2溶液,有白色沉淀生成,证明试样中含SO42- | |
| D. | 将Fe(NO3)2样品溶于稀硫酸,再滴加KSCN溶液变为红色,证明样品已部分或全部变质 |
分析 A.溶液变蓝,只能说明淀粉没有完全水解,无法判断是否水解;
B.氢氧化铝溶于氢氧化钠,应该向氯化铝、氯化铁溶液中滴加氢氧化钠溶液;
C.先与稀盐酸排除干扰离子,然后用氯化钡溶液检验是否含有硫酸根离子;
D.酸性条件下硝酸根离子能够氧化亚铁离子,干扰了检验结果.
解答 解:A.向淀粉水解后的溶液中加入碘水,溶液变蓝色,证明淀粉没有完全水解,应该用银氨溶液或新制氢氧化铜检验是否是否水解,故A错误;
B.向NaOH溶液中滴加浓度均为0.1mol•L-1的FeCl3和AlCl3混合溶液,由于氢氧化铝溶于氢氧化钠溶液,无法比较氢氧化铝和氢氧化铁的溶度积,应该向等浓度的氯化铁、氯化铝溶液中滴加氢氧化钠溶液,故B错误;
C.向待测试样中加入过量稀盐酸无现象,排除了碳酸根离子、银离子等干扰,再滴加BaCl2溶液,有白色沉淀生成,该沉淀为硫酸钡,则可证明试样中含SO42-,故C正确;
D.将Fe(NO3)2样品溶于稀硫酸,酸性条件下硝酸根离子具有强氧化性,将亚铁离子氧化成铁离子,干扰了检验,无法判断硝酸亚铁是否变质,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握淀粉水解原理、沉淀转化、离子检验方法为解答本题的关键,侧重分析与实验能力的考查,注意化学反应原理及实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
2.如图甲是利用一种微生物将废水中的尿素(H2NCONH2)的化学能直接转化为电能,并生成环境友好物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中不正确的是( )
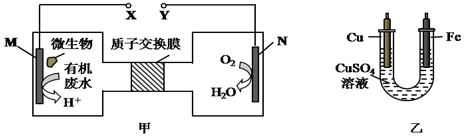

| A. | 铜电极应与Y相连接 | |
| B. | 乙装置中溶液的颜色不会变浅 | |
| C. | 当N电极消耗0.25 mol气体时,则铁电极质量增加16 g | |
| D. | M电极反应式:H2NCONH2+H2O-6e-═CO2↑+N2↑+6H+ |
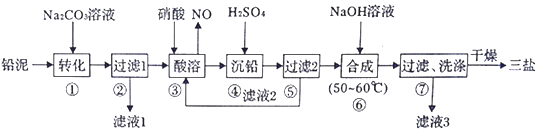
20.钴(Co)是重要的稀有金属,在工业和科技领域具有广泛的用途.从某含钴工业废料中回收钴的工艺流程如图:
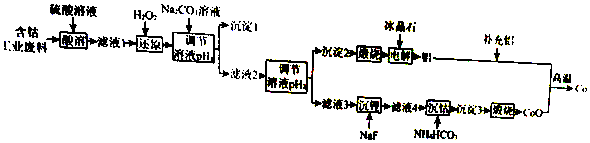
已知:
Ⅲ.离子浓度小于等于1.0×10-5mol•L-1时,认为该离子沉淀完全.
请回答下列问题:
(1)NaF的电子式为Na+[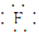 ]-.
]-.
(2)“沉淀1”的化学式为Fe(OH)3.“调节溶液pH2”的范围为4.7≤pH2<7.15.
(3)“还原”时发生反应的离子方程式为2CO3++H2O2=2CO2++O2↑2H+.“沉钴”时发生反应的离子方程式为CO2++2HCO3-=COCO3↓+CO2↑+H2O.
(4)制备Co时,“补充铝”的原因为原混合物中Al和Co的物质的量之比小于2:3.
(5)已知:l0-0.9≈0.13,则 A1(OH)3 的溶度积常数 Ksp=1.3×10-33.
(6)Li-SOCl2电池可用于心脏起搏器,该电池的总反应可表示为::4Li+2SOCl2═4LiCl+S+SO2,其正极反应式为2SOCl2+4e-=S+SO2+4Cl-.

已知:
| 含钴废料的成分 | |||||
| 成分 | Al | Li | Co2O3 | Fe2O3 | 其他不溶于强酸的杂质 |
| 质量分数/% | 10.5 | 0.35 | 65.6 | 9.6 | 13.95 |
| Ⅱ.实验中部分离子开始沉淀和沉淀完全的pH | |||
| 金属离子 | Fe3+ | Co2+ | Al3+ |
| 开始沉淀的pH | 1.9 | 7.15 | 3.4 |
| 沉淀完全的pH | 3.2 | 9.15 | 4.7 |
请回答下列问题:
(1)NaF的电子式为Na+[
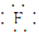 ]-.
]-.(2)“沉淀1”的化学式为Fe(OH)3.“调节溶液pH2”的范围为4.7≤pH2<7.15.
(3)“还原”时发生反应的离子方程式为2CO3++H2O2=2CO2++O2↑2H+.“沉钴”时发生反应的离子方程式为CO2++2HCO3-=COCO3↓+CO2↑+H2O.
(4)制备Co时,“补充铝”的原因为原混合物中Al和Co的物质的量之比小于2:3.
(5)已知:l0-0.9≈0.13,则 A1(OH)3 的溶度积常数 Ksp=1.3×10-33.
(6)Li-SOCl2电池可用于心脏起搏器,该电池的总反应可表示为::4Li+2SOCl2═4LiCl+S+SO2,其正极反应式为2SOCl2+4e-=S+SO2+4Cl-.
17.化学与生产、生活密切相关,下列说法正确的是( )
| A. | 冷浓硝酸不能用铝制容器盛装 | |
| B. | 钠可从钴盐溶液中置换出钴单质 | |
| C. | 食盐中加入碘单质可以预防甲状腺肿大 | |
| D. | 光导纤维遇氢氧化钠溶液易“断路” |
4.化学与科技、生活密切相关.下列说法错误的是( )
| A. | 肥皂水、矿泉水及食醋三种溶液的pH依次减小 | |
| B. | 高铁车厢采用的铝合金材料强度大、质量轻,不与氧气反应 | |
| C. | 食品袋中放入盛有硅胶和铁粉的透气小袋,是为了防止食物受潮、氧化变质 | |
| D. | 采用“静电除尘”、“汽车尾气催化净化”等方法可减少“雾霾”的发生 |
1.表为元素周期表的一部分,请回答下列问题:
(1)元素③在元素周期表中的位置是第二周期VA族.
(2)④和⑤两种元素的最高价氧化物对应水化物酸性较弱的是H2SO4(填化学式),②和④两种元素中,原子半径较大的是Al(填元素符号).
(3)元素①的氢氧化物与元素⑤的单质在常温下反应,化学方程式为:2NaOH+Cl2═NaCl+NaClO+H2O.
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ③ | |||||||
| 3 | ① | ② | ④ | ⑤ | ||||
(2)④和⑤两种元素的最高价氧化物对应水化物酸性较弱的是H2SO4(填化学式),②和④两种元素中,原子半径较大的是Al(填元素符号).
(3)元素①的氢氧化物与元素⑤的单质在常温下反应,化学方程式为:2NaOH+Cl2═NaCl+NaClO+H2O.