题目内容
某盐或“类盐”的化学式为XmYn(最简结构),将一定量的该盐溶于足量的水.
(1)若m≠n,测得该盐溶液的pH为5,则该盐与水反应的离子方程式可能为 .
(2)若m≠n,测得该盐溶液的pH为9,则该盐与水反应的离子方程式可能为 .
(3)若m≠n,X、Y为同周期的短周期元素,XmYn溶于水时,既有白色沉淀生成,又有无色气体放出,则该物质溶于水的化学方程式为 .
(4)若X、Y为同主族的短周期元素,且m=n,则该物质溶于水的化学方程式为 .
(1)若m≠n,测得该盐溶液的pH为5,则该盐与水反应的离子方程式可能为
(2)若m≠n,测得该盐溶液的pH为9,则该盐与水反应的离子方程式可能为
(3)若m≠n,X、Y为同周期的短周期元素,XmYn溶于水时,既有白色沉淀生成,又有无色气体放出,则该物质溶于水的化学方程式为
(4)若X、Y为同主族的短周期元素,且m=n,则该物质溶于水的化学方程式为
考点:盐类水解的原理,化学方程式的书写
专题:
分析:(1)若测得溶液的pH为5,溶液呈酸性,说明阳离子水解;
(2)若测得盐溶液的pH为9,溶液呈碱性,阴离子水解;
(3)X、Y为同周期的短周期元素,XmYn溶于水时,有白色沉淀产生,又有无色气体放出说明阴离子和阳离子都能水解;
(4)若X、Y为同主族的短周期元素,且m=n,则X、Y的化合价的绝对值相等,二者一种为金属另一种为非金属,只有第IA主族的H和Na符合,则为NaH.
(2)若测得盐溶液的pH为9,溶液呈碱性,阴离子水解;
(3)X、Y为同周期的短周期元素,XmYn溶于水时,有白色沉淀产生,又有无色气体放出说明阴离子和阳离子都能水解;
(4)若X、Y为同主族的短周期元素,且m=n,则X、Y的化合价的绝对值相等,二者一种为金属另一种为非金属,只有第IA主族的H和Na符合,则为NaH.
解答:
解:(1)若测得溶液的pH为5,溶液呈酸性,说明阳离子水解,离子方程式可能为:Xn-+nH2O?X(OH)n+nH+,故答案为:Xn-+nH2O?X(OH)n+nH+;
(2)pH为9说明溶液呈碱性,阴离子水解,离子方程式可能为::Ym-+H2O?HY(m-1)-+OH-,故答案为:Ym-+H2O?HY(m-1)-+OH-;
(2)X、Y为同周期的短周期元素,XmYn溶于水时,有白色沉淀产生,又有无色气体放出说明阴离子和阳离子都能水解;则XmYn为Al2S3,XmYn溶于水的化学方程式为:Al2S3+6H2O=2Al(OH)3↓+3H2S↑,故答案为:Al2S3+6H2O=2Al(OH)3↓+3H2S↑;
(4)若X、Y为同主族的短周期元素,且m=n,则X、Y的化合价的绝对值相等,二者一种为金属另一种为非金属,只有第IA主族的H和Na符合,则为NaH,NaH与水反应生成氢气和氢氧化钠,其反应的方程式为2NaH+2H2O=2NaOH+H2↑,故答案为:2NaH+2H2O=2NaOH+H2↑.
(2)pH为9说明溶液呈碱性,阴离子水解,离子方程式可能为::Ym-+H2O?HY(m-1)-+OH-,故答案为:Ym-+H2O?HY(m-1)-+OH-;
(2)X、Y为同周期的短周期元素,XmYn溶于水时,有白色沉淀产生,又有无色气体放出说明阴离子和阳离子都能水解;则XmYn为Al2S3,XmYn溶于水的化学方程式为:Al2S3+6H2O=2Al(OH)3↓+3H2S↑,故答案为:Al2S3+6H2O=2Al(OH)3↓+3H2S↑;
(4)若X、Y为同主族的短周期元素,且m=n,则X、Y的化合价的绝对值相等,二者一种为金属另一种为非金属,只有第IA主族的H和Na符合,则为NaH,NaH与水反应生成氢气和氢氧化钠,其反应的方程式为2NaH+2H2O=2NaOH+H2↑,故答案为:2NaH+2H2O=2NaOH+H2↑.
点评:本题考查了盐类水解的分析应用、方程式的书写等,明确溶液显酸碱性的原因是解题的关键,注意把握常见的能发生相互促进的水解的离子,题目难度中等.

练习册系列答案
相关题目
下列离子方程式书写不正确的是( )
| A、NaHSO4溶液与Ba(OH)2溶液混合后溶液呈中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
| B、将标准状况下336 mL氯气通入10 mL 1 mol?L-1的溴化亚铁溶液中:2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2 |
| C、次氯酸钙溶液中通入过量二氧化硫:Ca(ClO)2+H2O+SO2=CaSO3↓+2HClO |
| D、向澄清石灰水中加入过量的碳酸氢钠溶液:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32- |
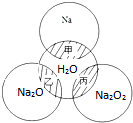 如图所示,两圆圈相交的阴影部分甲、乙、丙表示圆圈内物质相互发生的反应,钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )
如图所示,两圆圈相交的阴影部分甲、乙、丙表示圆圈内物质相互发生的反应,钠及其氧化物的物质的量均为0.1mol,水的质量为100g.下列说法正确的是( )| A、甲、乙、丙都属于氧化还原反应 |
| B、丙反应中的氧化剂是Na2O2,还原剂时H2O |
| C、丙反应中消耗1molNa2O2,则转移1mol电子 |
| D、若甲、乙、丙反应后所得溶液的质量分数分别为w1、w2、w3,则:2w1=w2=w3 |
一定条件下,通过下列反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g)
2CO2(g)+S(s),若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
| ||
| A、从平衡混合气体中分离出CO2可增大平衡常数K |
| B、平衡后,其他条件不变,加入硫,逆反应速率加快 |
| C、平衡后,若升高温度,CO体积分数增大,则正反应的△H<0 |
| D、平衡后,其他条件不变,通入CO2,该反应的△H减小 |
NA表示阿伏伽德罗常数,下列判断正确的是( )
| A、在20gD216O中含有10NA个电子 |
| B、标准情况下,2.24L己烷所含分子数为0.1NA |
| C、1molCl2参加反应时转移电子数一定为2NA |
| D、含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol/L |
下列粒子在化学反应中既能表现氧化性又能表现还原性的是( )
| A、S2- |
| B、Al3+ |
| C、H2O2 |
| D、K |