题目内容
可逆反应:2NO2?2NO+O2在密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②体积可变的容器中压强不再变化的状态
③体积可变的容器中混合气体的平均相对分子质量不再改变的状态
④体积不变的容器中混合气体的颜色不再改变的状态
⑤体积不变的容器中混合气体的密度不再改变的状态
⑥用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态.
①单位时间内生成n mol O2的同时生成2n mol NO2
②体积可变的容器中压强不再变化的状态
③体积可变的容器中混合气体的平均相对分子质量不再改变的状态
④体积不变的容器中混合气体的颜色不再改变的状态
⑤体积不变的容器中混合气体的密度不再改变的状态
⑥用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态.
| A、①④⑥ | B、②③⑤ |
| C、①③④ | D、①④⑤ |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:可逆反应达到平衡状态时,正逆反应速率相等(同种物质)或正逆反应速率之比等于系数之比(不同物质),平衡时各种物质的物质的量、浓度等不再发生变化,由此衍生的一些物理量不变,以此分析.
解答:
解:①单位时间内生成n mol O2,同时生成2n molNO2,说明反应v正=v逆,达到平衡状态,故①正确;
②体积可变的容器中压强始终不变,所以不能根据压强来判断平衡状态,故②错误;
③反应后气体的物质的量增大,混合气体的质量不变,所以混合气体的平均相对分子质量逐渐减小,当混合气体的平均相对分子质量不再改变时即是平衡状态,故③正确;
④混合气体的颜色不再改变,说明NO2气体的浓度不变,达到平衡状态,故④正确;
⑤体积不变的容器中,气体的体积不变,气体的质量守恒,所以混合气体的密度始终不变,所以不能根据密度来判断平衡状态,故⑤错误;
⑥反应速率之比等于各物质的计量数比始终成立,所以用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态不一定是平衡状态,故⑥错误;
所以正确的有①③④.
故选:C.
②体积可变的容器中压强始终不变,所以不能根据压强来判断平衡状态,故②错误;
③反应后气体的物质的量增大,混合气体的质量不变,所以混合气体的平均相对分子质量逐渐减小,当混合气体的平均相对分子质量不再改变时即是平衡状态,故③正确;
④混合气体的颜色不再改变,说明NO2气体的浓度不变,达到平衡状态,故④正确;
⑤体积不变的容器中,气体的体积不变,气体的质量守恒,所以混合气体的密度始终不变,所以不能根据密度来判断平衡状态,故⑤错误;
⑥反应速率之比等于各物质的计量数比始终成立,所以用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态不一定是平衡状态,故⑥错误;
所以正确的有①③④.
故选:C.
点评:本题考查化学平衡状态的判断,题目难度不大,做题时注意分析化学方程式的前后计量数大小的关系.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
在强酸性溶液中能大量共存,并且溶液为无色透明的离子组是( )
| A、NH4+、Al3+、SO42-、NO3- |
| B、K+、NH4+、MnO4-、SO42- |
| C、Na+、OH-、NO3-、HCO3- |
| D、K+、Cu2+、CH3COO-、NO3- |
下列说法不正确的是( )
| A、假说经过反复验证和修正,才发展成为科学的理论 |
| B、化学模型在研究物质的结构和性质变化时有很重要的作用 |
| C、研究物质的性质常用观察、实验、分类、比较等方法 |
| D、探究物质性质的基本程序是做实验并观察实验现象→分析、解释,得出结论 |
下列物质是电解质的是( )
| A、稀硫酸 | B、熔融的氯化钠 |
| C、酒精 | D、铜 |
下列各组物质按酸碱盐分类顺序排列,正确的是( )
| A、硫酸、纯碱、硫酸钙 |
| B、氢硫酸、烧碱、胆矾 |
| C、碳酸、乙醇、醋酸钠 |
| D、磷酸、熟石灰、苛性钠 |
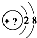 某同学在画某种元素的一种单核微粒的结构示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断.
某同学在画某种元素的一种单核微粒的结构示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断.
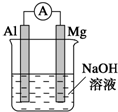 将镁条、铝条平行插入盛有一定浓度NaOH溶液的烧杯中,用导线和电流表连接成原电池,装置如图所示.此电池工作时,下列叙述正确的是( )
将镁条、铝条平行插入盛有一定浓度NaOH溶液的烧杯中,用导线和电流表连接成原电池,装置如图所示.此电池工作时,下列叙述正确的是( )