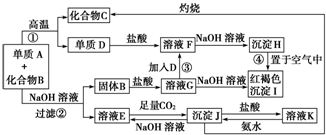
题目内容
按要求填空
(1)在化学反应中,如果反应前后元素化合价发生变化,就一定有 转移.元素化合价升高,表明该元素的原子 电子,含该元素的物质发生 反应,这种物质是 剂.
(2)黑火药在发生爆炸时,发生如下的反应:2KNO3+3C+S═K2S+N2↑+3CO2↑.其中被还原的元素是 ,被氧化的元素是 ,氧化剂是
(3)现有下列8中物质:①H2 ②空气 ③Mg ④CaO ⑤盐酸 ⑥Ca(OH)2⑦CuSO4?5H2O ⑧碘酒 其中,属于混合物的是 ;属于氧化物的是 ;属于盐的是 ;属于电解质的是 .
(4)写出Fe2(SO4)3的电离方程式
(5)写出与2H++CO32-═H2O+CO2↑相对的化学方程式
(6)用双线桥标出下列反应中电子转移的方向和数目 ,并指出氧化剂和还原剂.Cl2+SO2+2H2O═H2SO4+2HCl
氧化剂: ,还原剂: ;
(7)用饱和NaHCO3溶液除去混在CO2中少量的HCl气体,其反应的离子方程式 .
(1)在化学反应中,如果反应前后元素化合价发生变化,就一定有
(2)黑火药在发生爆炸时,发生如下的反应:2KNO3+3C+S═K2S+N2↑+3CO2↑.其中被还原的元素是
(3)现有下列8中物质:①H2 ②空气 ③Mg ④CaO ⑤盐酸 ⑥Ca(OH)2⑦CuSO4?5H2O ⑧碘酒 其中,属于混合物的是
(4)写出Fe2(SO4)3的电离方程式
(5)写出与2H++CO32-═H2O+CO2↑相对的化学方程式
(6)用双线桥标出下列反应中电子转移的方向和数目
氧化剂:
(7)用饱和NaHCO3溶液除去混在CO2中少量的HCl气体,其反应的离子方程式
考点:氧化还原反应,酸、碱、盐、氧化物的概念及其相互联系
专题:物质的分类专题,氧化还原反应专题
分析:(1)氧化还原反应的特征为化合价的变化,本质为电子转移,含元素化合价升高的物质为还原剂;
(2)2KNO3+3C+S═K2S+N2↑+3CO2↑中,N、S元素的化合价降低,C元素的化合价升高;
(3)①H2只有一种元素组成,为单质,既不是电解质也不是非电解质;
②空气中含氧气、氮气等物质,为混合物,既不是电解质也不是非电解质;
③Mg只有一种元素组成,为单质,既不是电解质也不是非电解质;
④CaO含Ca、O元素,为氧化物,且在熔融状态导电,为电解质;
⑤盐酸为HCl的水溶液,为混合物,既不是电解质也不是非电解质;
⑥Ca(OH)2由金属离子和氢氧根离子构成,为碱,且在熔融状态或溶于水导电,为电解质;
⑦CuSO4?5H2O由金属离子、酸根离子构成,为盐,且在熔融状态或溶于水导电,为电解质;
⑧碘酒为酒精、碘的混合物,既不是电解质也不是非电解质;
(4)Fe2(SO4)3为强电解质,完全电离;
(5)强酸与可溶性碳酸盐生成可溶性盐、水、二氧化碳的离子反应为2H++CO32-═H2O+CO2↑;
(6)Cl2+SO2+2H2O═H2SO4+2HCl中,Cl元素的化合价降低,S元素的化合价升高,转移2e-;
(7)NaHCO3与HCl反应生成NaCl、水、二氧化碳.
(2)2KNO3+3C+S═K2S+N2↑+3CO2↑中,N、S元素的化合价降低,C元素的化合价升高;
(3)①H2只有一种元素组成,为单质,既不是电解质也不是非电解质;
②空气中含氧气、氮气等物质,为混合物,既不是电解质也不是非电解质;
③Mg只有一种元素组成,为单质,既不是电解质也不是非电解质;
④CaO含Ca、O元素,为氧化物,且在熔融状态导电,为电解质;
⑤盐酸为HCl的水溶液,为混合物,既不是电解质也不是非电解质;
⑥Ca(OH)2由金属离子和氢氧根离子构成,为碱,且在熔融状态或溶于水导电,为电解质;
⑦CuSO4?5H2O由金属离子、酸根离子构成,为盐,且在熔融状态或溶于水导电,为电解质;
⑧碘酒为酒精、碘的混合物,既不是电解质也不是非电解质;
(4)Fe2(SO4)3为强电解质,完全电离;
(5)强酸与可溶性碳酸盐生成可溶性盐、水、二氧化碳的离子反应为2H++CO32-═H2O+CO2↑;
(6)Cl2+SO2+2H2O═H2SO4+2HCl中,Cl元素的化合价降低,S元素的化合价升高,转移2e-;
(7)NaHCO3与HCl反应生成NaCl、水、二氧化碳.
解答:
解:(1)在化学反应中,如果反应前后元素化合价发生变化,就一定有电子转移,元素化合价升高,表明该元素的原子失去电子,含该元素的物质发生氧化反应,这种物质是还原剂,
故答案为:电子;失去;氧化;还原;
(2)2KNO3+3C+S═K2S+N2↑+3CO2↑中,N、S元素的化合价降低,C元素的化合价升高,则N、S元素被还原,氧化剂为KNO3、S,C元素被氧化,
故答案为:N、S;C;KNO3、S;
(3)①H2只有一种元素组成,为单质,既不是电解质也不是非电解质;
②空气中含氧气、氮气等物质,为混合物,既不是电解质也不是非电解质;
③Mg只有一种元素组成,为单质,既不是电解质也不是非电解质;
④CaO含Ca、O元素,为氧化物,且在熔融状态导电,为电解质;
⑤盐酸为HCl的水溶液,为混合物,既不是电解质也不是非电解质;
⑥Ca(OH)2由金属离子和氢氧根离子构成,为碱,且在熔融状态或溶于水导电,为电解质;
⑦CuSO4?5H2O由金属离子、酸根离子构成,为盐,且在熔融状态或溶于水导电,为电解质;
⑧碘酒为酒精、碘的混合物,既不是电解质也不是非电解质,
属于混合物的是②⑤⑧,属于氧化物的是④,属于盐的是⑦,属于电解质的是④⑥⑦,
故答案为:②⑤⑧;④;⑦;④⑥⑦;
(4)Fe2(SO4)3为强电解质,完全电离,电离方程式为Fe2(SO4)3=2Fe3++3SO42-,故答案为:Fe2(SO4)3=2Fe3++3SO42-;
(5)强酸与可溶性碳酸盐生成可溶性盐、水、二氧化碳的离子反应为2H++CO32-═H2O+CO2↑,如2HCl+Na2CO3═H2O+CO2↑+2NaCl,
故答案为:2HCl+Na2CO3═H2O+CO2↑+2NaCl;
(6)Cl2+SO2+2H2O═H2SO4+2HCl中,Cl元素的化合价降低,S元素的化合价升高,转移2e-,所以Cl2是氧化剂、SO2是还原剂,转移电子数目和方向为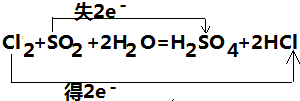 ,故答案为:
,故答案为: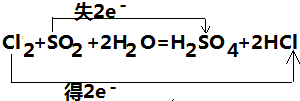 ;Cl2;SO2;
;Cl2;SO2;
(7)NaHCO3与HCl反应生成NaCl、水、二氧化碳,离子反应为H++HCO3-═H2O+CO2↑,故答案为:H++HCO3-═H2O+CO2↑.
故答案为:电子;失去;氧化;还原;
(2)2KNO3+3C+S═K2S+N2↑+3CO2↑中,N、S元素的化合价降低,C元素的化合价升高,则N、S元素被还原,氧化剂为KNO3、S,C元素被氧化,
故答案为:N、S;C;KNO3、S;
(3)①H2只有一种元素组成,为单质,既不是电解质也不是非电解质;
②空气中含氧气、氮气等物质,为混合物,既不是电解质也不是非电解质;
③Mg只有一种元素组成,为单质,既不是电解质也不是非电解质;
④CaO含Ca、O元素,为氧化物,且在熔融状态导电,为电解质;
⑤盐酸为HCl的水溶液,为混合物,既不是电解质也不是非电解质;
⑥Ca(OH)2由金属离子和氢氧根离子构成,为碱,且在熔融状态或溶于水导电,为电解质;
⑦CuSO4?5H2O由金属离子、酸根离子构成,为盐,且在熔融状态或溶于水导电,为电解质;
⑧碘酒为酒精、碘的混合物,既不是电解质也不是非电解质,
属于混合物的是②⑤⑧,属于氧化物的是④,属于盐的是⑦,属于电解质的是④⑥⑦,
故答案为:②⑤⑧;④;⑦;④⑥⑦;
(4)Fe2(SO4)3为强电解质,完全电离,电离方程式为Fe2(SO4)3=2Fe3++3SO42-,故答案为:Fe2(SO4)3=2Fe3++3SO42-;
(5)强酸与可溶性碳酸盐生成可溶性盐、水、二氧化碳的离子反应为2H++CO32-═H2O+CO2↑,如2HCl+Na2CO3═H2O+CO2↑+2NaCl,
故答案为:2HCl+Na2CO3═H2O+CO2↑+2NaCl;
(6)Cl2+SO2+2H2O═H2SO4+2HCl中,Cl元素的化合价降低,S元素的化合价升高,转移2e-,所以Cl2是氧化剂、SO2是还原剂,转移电子数目和方向为
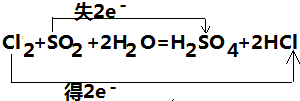 ,故答案为:
,故答案为: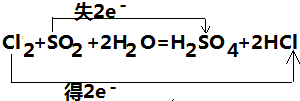 ;Cl2;SO2;
;Cl2;SO2;(7)NaHCO3与HCl反应生成NaCl、水、二氧化碳,离子反应为H++HCO3-═H2O+CO2↑,故答案为:H++HCO3-═H2O+CO2↑.
点评:本题考查较综合,涉及氧化还原反应、离子反应及物质分类等,为高考高频考点,把握发生的化学反应及化学用语的使用为解答的关键,侧重基础知识和分析应用能力的考查,题目难度不大.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
下列关于淀粉的说法不正确的是( )
| A、淀粉不溶于水 |
| B、淀粉属于高分子化合物 |
| C、淀粉在人体内能够水解 |
| D、淀粉与碘作用呈蓝色 |
现有常温下的四种溶液(如下表),下列有关叙述中正确的是( )
| ① | ② | ③ | ④ | |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
| A、V1L④与V2L②溶液混合后,若混合后溶液pH=4,则V1:V2=9:11 |
| B、将①、④两种溶液等体积混合,所得溶液中:c (NH4+)>c(Cl-)>c(OH-)>c(H+) |
| C、分别加水稀释10倍、四种溶液的pH:①>②>③>④ |
| D、在①、②中分别加入适量的氯化铵晶体后,①的pH减小,②的pH不变 |