题目内容
下列有关化学反应过程或实验现象的叙述中,正确的是( )
| A、氯气的水溶液可以导电,说明氯气是电解质 |
| B、漂白粉和明矾都常用于自来水的处理,但二者的作用原理是不相同的 |
| C、氯气可以使湿润的有色布条褪色,但实际起漂白作用的物质是次氯酸而不是氯气 |
| D、为证明氯水中含Cl-,可先加盐酸酸化,再加入AgNO3溶液 |
考点:氯气的化学性质
专题:卤族元素
分析:A、水溶液中或熔融状态导电的化合物为电解质分析判断;
B、漂白粉利用强氧化性消毒杀菌,明矾石利用铝离子水解生成的氢氧化铝胶体具有吸附杂质作用净水;
C、氯气无漂白性,起漂白性的是次氯酸;
D、加入盐酸含有氯离子移向氯离子的检验判断.
B、漂白粉利用强氧化性消毒杀菌,明矾石利用铝离子水解生成的氢氧化铝胶体具有吸附杂质作用净水;
C、氯气无漂白性,起漂白性的是次氯酸;
D、加入盐酸含有氯离子移向氯离子的检验判断.
解答:
解:A、电解质必须是化合物,氯气是单质,故A错误;
B、漂白粉是利用强氧化性消毒,而明矾净水是利用Al3+水解生成的Al(OH)3胶体吸附杂质,二者的作用原理是不相同,故B正确;
C、氯气可以使湿润的有色布条褪色,是因为Cl2+H2O=HClO+HCl,次氯酸具有漂白作用,氯气无漂白性,故C正确;
D、加盐酸时引入Cl-,干扰实验,故D错误;
故选BC.
B、漂白粉是利用强氧化性消毒,而明矾净水是利用Al3+水解生成的Al(OH)3胶体吸附杂质,二者的作用原理是不相同,故B正确;
C、氯气可以使湿润的有色布条褪色,是因为Cl2+H2O=HClO+HCl,次氯酸具有漂白作用,氯气无漂白性,故C正确;
D、加盐酸时引入Cl-,干扰实验,故D错误;
故选BC.
点评:本题考查了氯气的性质分析判断,注意漂白性的物质判断,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
在1L定容的密闭容器中,可以证明可逆反应N2+3H2? 2NH3 已达到平衡状态的是( )
| A、c(N2):c(H2):c(NH3)=1:3:2 |
| B、一个N≡N 断裂的同时,有3个H-H生成 |
| C、其他条件不变时,混合气体的密度不再改变 |
| D、v正(N2)═2 v逆(NH3) |
采用下列装置和操作,能达到实验目的是( )
A、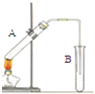 A中为乙醇、醋酸,B中为饱和碳酸钠溶液,制取乙酸乙酯 |
B、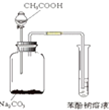 验证醋酸、碳酸、苯酚的酸性强弱 |
C、 用浓硫酸、乙醇共热到约170℃制乙烯 |
D、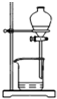 用NaOH溶液除去苯中混有的少量苯酚 |
进行化学实验时必须要有安全意识,下列做法错误的是( )
| A、被玻璃割伤手后,先取出伤口里的玻璃片,再用稀过氧化氢溶液擦洗,然后敷药包扎 |
| B、加热试管时不小心发生烫伤,第一时间用冷水冲洗,再涂食盐(始终保持湿润)消毒降温 |
| C、温度计摔坏导致水银散落到地面上,应立即用水冲洗水银 |
| D、滴瓶中的滴管用后不用清洗,直接放到滴瓶中 |
将0.1molN2O4置于密闭烧瓶中,把烧瓶放入100℃的恒温水浴,烧瓶内气体逐渐变为红棕色:N2O4(g)?2NO2 (g),能说明反应在该条件下达到平衡状态的是( )
| A、N2O4的消耗速率与NO2的生成速率相等 |
| B、烧瓶内气体的颜色不再变化 |
| C、烧瓶内混合气体的质量不再变化 |
| D、烧瓶内混合气体的压强不再变化 |
下列各组物理量中,随取水量的变化而变化的是( )
| A、水的沸点 |
| B、水的密度 |
| C、水的物质的量 |
| D、水的摩尔质量 |
水溶液中能大量共存的一组离子是( )
| A、Al3+、Na+、CO32-、NO3- |
| B、Ag+、Cl-、Fe3+、HCO3- |
| C、Fe2+、H+、K+、MnO4- |
| D、Mg2+、Br-、NH4+、SO42- |