题目内容
五种短周期元素(用字母表示)在周期表中的相对位置如下,其中Y的单质在空气中含量最高.下列判断正确的是( )
| X | Y | ||
| Z | M | R |
| A、气态氢化物稳定性:X>Y |
| B、最高价氧化物的水化物的酸性:Y>M |
| C、R的氧化物的水化物是离子化合物 |
| D、Z、M、R的原子半径依次减小,最高化合价依次升高 |
考点:位置结构性质的相互关系应用,元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:Y的单质在空气中含量最高,则Y为N,由位置关系可知,X为C,Z为Al,M为P,R为S,
A.非金属性越强,气态氢化物越稳定;
B.非金属性越强,最高价氧化物的水化物的酸性越强;
C.R的氧化物的水化物,为硫酸或亚硫酸;
D.同周期原子序数大的半径小,Z、M、R的最高化合价分别为+3、+5、+6.
A.非金属性越强,气态氢化物越稳定;
B.非金属性越强,最高价氧化物的水化物的酸性越强;
C.R的氧化物的水化物,为硫酸或亚硫酸;
D.同周期原子序数大的半径小,Z、M、R的最高化合价分别为+3、+5、+6.
解答:
解:Y的单质在空气中含量最高,则Y为N,由位置关系可知,X为C,Z为Al,M为P,R为S,
A.非金属性Y>X,气态氢化物稳定性:X<Y,故A错误;
B.非金属性Y>M,最高价氧化物的水化物的酸性:Y>M,故B正确;
C.R的氧化物的水化物,为硫酸或亚硫酸,只含共价键,为共价化合物,故C错误;
D.同周期原子序数大的半径小,Z、M、R的最高化合价分别为+3、+5、+6,则Z、M、R的原子半径依次减小,最高化合价依次升高,故D正确;
故选BD.
A.非金属性Y>X,气态氢化物稳定性:X<Y,故A错误;
B.非金属性Y>M,最高价氧化物的水化物的酸性:Y>M,故B正确;
C.R的氧化物的水化物,为硫酸或亚硫酸,只含共价键,为共价化合物,故C错误;
D.同周期原子序数大的半径小,Z、M、R的最高化合价分别为+3、+5、+6,则Z、M、R的原子半径依次减小,最高化合价依次升高,故D正确;
故选BD.
点评:本题考查位置、结构及性质的应用,把握Y为金属N元素并推出各元素为解答的关键,注意元素周期律的应用及非金属性的比较方法,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
几种短周期元素的原子半径及主要化合价如下表,由此可知( )
| 元素代号 | X | Y | Z | W |
| 原子半径/nm | 0.186 | 0.089 | 0.074 | 0.099 |
| 主要化合价 | +1 | +2 | -2 | +7、-1 |
| A、X、Y元素的金属性:X<Y |
| B、X、Z形成的化合物中一定不含共价键 |
| C、W的最高价氧化物的水化物是一种强酸 |
| D、离子半径:X+>Z2- |
下列装置或操作能达到所注明的实验能达到实验目的是( )
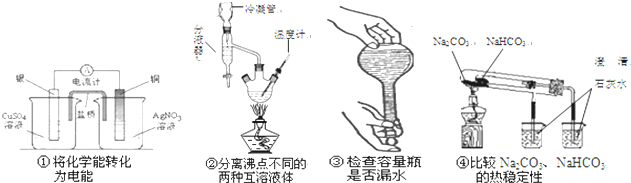

| A、①② | B、③④ | C、①③ | D、②④ |
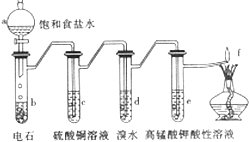 如图是制备和研究乙炔性质的实验装置图.下列说法不正确的是( )
如图是制备和研究乙炔性质的实验装置图.下列说法不正确的是( )| A、制备乙炔的反应原理是:CaC2+2H2O→Ca(OH)2+C2H2↑ |
| B、c的作用是除去影响后续实验的杂质 |
| C、d中的有机产物与AgNO3溶液混合能产生沉淀 |
| D、e中的现象说明乙炔能被高锰酸钾酸性溶液氧化 |
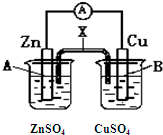 某电化学装置如图所示,下列说法正确的是( )
某电化学装置如图所示,下列说法正确的是( )| A、若X是盐桥,则电子由B电极经外电路流向A电极 |
| B、若X是盐桥,取出X电流表指针仍然偏转 |
| C、若X是锌条,则A电极的质量会减少 |
| D、若X是铜条,则A电极的电极反应式是:Zn2++2e-=Zn |
下列说法正确的是( )
| A、温室效应是当今世界面临的环境问题,使温室效应增强的气体只有二氧化碳 |
| B、直馏汽油、裂化汽油、植物油、甘油均能与溴发生加成反应而使溴的四氯化碳溶液褪色 |
| C、PX(对二甲苯)是制造聚酯纤维的原料,它是一种难溶于水密度比水大的剧毒物质 |
| D、晶体硅可用于制作太阳能电池板,二氧化硅可用于制作光导纤维 |
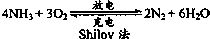 以氨气代替氢气来研发氨燃料电池是当前科研的一个热点.氨燃料电池使用的电解质溶液是KOH溶液,电池反应如图:有关下列说法错误的是( )
以氨气代替氢气来研发氨燃料电池是当前科研的一个热点.氨燃料电池使用的电解质溶液是KOH溶液,电池反应如图:有关下列说法错误的是( )| A、氨燃料电池在充电时,OH-向电池的负极移动 |
| B、氨燃料电池在放电时,负极反应为:2NH3-6e-+6OH-═N2+6H2O |
| C、以氨气代替氢气的主要原因是:氨气易液化易储存 |
| D、燃料电池的能量转化率一般比普通的电池高 |
下列对应关系正确的是( )
| A | B | C | D |
 |
 |
 |
 |
| 浓硫酸 | 氢氧化钠 | 废旧灯管 | 废旧易拉罐 |
| A、A | B、B | C、C | D、D |