题目内容
8.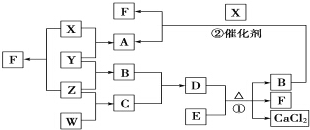 X、Y、Z、W均为气体单质,A、B、C均为无色气体化合物,D、E均为白色固体,F在通常情况下为无色无味的液体,它们有如下的转化关系:
X、Y、Z、W均为气体单质,A、B、C均为无色气体化合物,D、E均为白色固体,F在通常情况下为无色无味的液体,它们有如下的转化关系:请回答下列问题:
(1)Y分子的电子式为
 ,F中的化学键类型为共价键.
,F中的化学键类型为共价键.(2)C的化学式为HCl.
(3)B在F中的反应可以表示为NH3+H2O?NH3•H2O?NH4++OH-.
(4)写出反应①和②的化学方程式:①2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;②4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
分析 X、Y、Z、W均为气体单质,F在通常情况下为无色无味的液体,X与Z反应得到F,则F为H2O,X、Z分别为H2、O2中的一种,A、B、C均为无色气体化合物,D、E均为白色固体,反应①是实验式制备氨气,则B为NH3,D、E分别为NH4Cl、Ca(OH)2中的一种,B与X反应得到A与F(水),则X为O2,A为NO,Z为H2,X与Y反应得到A,故Y为N2,B(氨气)与C反应得到D,则D为NH4Cl、E为Ca(OH)2、C为HCl,而气体单质W与Z反应得到C,故W为Cl2,据此解答.
解答 解:X、Y、Z、W均为气体单质,F在通常情况下为无色无味的液体,X与Z反应得到F,则F为H2O,X、Z分别为H2、O2中的一种,A、B、C均为无色气体化合物,D、E均为白色固体,反应①是实验式制备氨气,则B为NH3,D、E分别为NH4Cl、Ca(OH)2中的一种,B与X反应得到A与F(水),则X为O2,A为NO,Z为H2,X与Y反应得到A,故Y为N2,B(氨气)与C反应得到D,则D为NH4Cl、E为Ca(OH)2、C为HCl,而气体单质W与Z反应得到C,故W为Cl2.
(1)Y为N2,电子式为 ,F为H2O,含有的化学键类型为共价键,故答案为:
,F为H2O,含有的化学键类型为共价键,故答案为: ;共价键;
;共价键;
(2)C的化学式为HCl 故答案为:HCl;
(3)B在F中的反应可以表示为:NH3+H2O?NH3•H2O?NH4++OH-,故答案为:NH3+H2O?NH3•H2O?NH4++OH-;
(4)反应①的化学方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,反应②的化学方程式:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
点评 本题考查无机物推断,题目涉及物质比较多,熟练掌握气体的实验室制备与常见化学工业、元素化合物性质,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 三种气体质量相等 | B. | 三种气体的物质的量之比为16:2:1 | ||
| C. | 三种气体压强比为16:2:1 | D. | 三种气体体积比为1:8:16 |
| A. | 两溶液中水的电离程度相同 | B. | 水的离子积常数为1.0×10-(a+b) | ||
| C. | CH3COOH的电离常数为$\frac{(1{0}^{-2a})}{c}$ | D. | 两溶液中c(CH3COO-)=c(NH4+) |
根据上述实验,下列说法正确的是( )
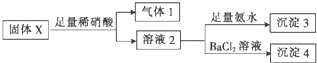
| A. | 气体1可能为SO2和CO2的混合物 | |
| B. | 沉淀3可能为Mg(OH)2和Al(OH)3的混合物 | |
| C. | 沉淀4可能为BaCO3、BaSO3或二者混合物 | |
| D. | 固体粉末X中一定有Na2CO3,可能有KAlO2 |
| A. | 鉴别Na2CO3和NaHCO3可用Ba(OH)2或Ca(OH)2溶液 | |
| B. | 除去Na2CO3固体中混有的少量NaHCO3,可采用加热法 | |
| C. | CO2中混有少量HCl、SO2等气体时,可用饱和NaHCO3溶液提纯气体 | |
| D. | 将澄清石灰水滴入NaHCO3溶液中,开始时发生反应的离子方程式为:Ca2++2OH-+2HCO3-═CaCO3↓+CO32-+2H2O |
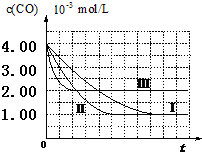 (I)目前,汽车厂商常利用催化技术将尾气中的NO和CO转化成CO2和N2,化学方程式如下:2NO+2CO$\stackrel{催化剂}{?}$2CO2+N2.为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究.
(I)目前,汽车厂商常利用催化技术将尾气中的NO和CO转化成CO2和N2,化学方程式如下:2NO+2CO$\stackrel{催化剂}{?}$2CO2+N2.为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究.【资料查阅】①不同的催化剂对同一反应的催化效率不同;
②使用相同的催化剂,当催化剂质量相等时,催化剂的比表面积对催化效率有影响.
【实验设计】课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验.
(1)完成以下实验设计表(表中不要留空格).
| 实验编号 | 实验目的 | T/℃ | NO初始浓度mol/L | CO初始浓度mol/L | 同种催化剂的比表面积m2/g |
| Ⅰ | 为以下实验作参照 | 280 | 6.50×10-3 | 4.00×10-3 | 80 |
| Ⅱ | 探究催化剂比表面积对尾气转化速率的影响 | 6.50×10-3 | 4.00×10-3 | 120 | |
| Ⅲ | 探究温度对尾气转化速率的影响 | 360 | 6.50×10-3 | 4.00×10-3 | 80 |
(2)计算第Ⅰ组实验中,达平衡时NO的浓度为3.5×10-3mol/L;
(3)由曲线Ⅰ、Ⅱ可知,增大催化剂比表面积,汽车尾气转化速率增大(填“增大”、“减小”、“无影响”).
(II)随着世界粮食需求量的增长,农业对化学肥料的需求量越来越大,其中氮肥是需求量最大的一种化肥.而氨的合成为氮肥的生产工业奠定了基础,其原理为:N2+3H2?2NH3
(1)在N2+3H2?2NH3的反应中,一段时间后,NH3的浓度增加了0.9mol•L-1.用N2表示其反应速率为0.15mol•L-1•s-1,则所经过的时间为B;
A.2s B.3s C.4s D.6s
(2)下列4个数据是在不同条件下测得的合成氨反应的速率,其中反应最快的是D.
A.v(H2)=0.1mol•L-1•min-1 B.v(N2)=0.1mol•L-1•min-1
C.v(NH3)=0.15mol•L-1•min-1 D.v(N2)=0.002mol•L-1•s-1.
| A. | 熔融的NaOH | B. | 液态HCl | C. | KCl溶液 | D. | 蔗糖溶液 |
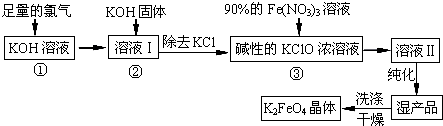
 .
.