题目内容
下列装置或操作正确(部分仪器已省略),且能达到实验目的是( )
| 选项 | A | B | C | D |
| 装置或操作 |  |
 |
 |
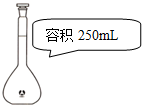 |
| 实验目的 | 石油的蒸馏 | 除去Cl2中的HCl | 存放液溴 | 配制240mL 0.1mol/L的NaCl溶液 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.温度计位置错误;
B.氯气和氢氧化钠溶液反应;
C.溴腐蚀橡胶塞;
D.可用250mL容量瓶配制体积略小的溶液.
B.氯气和氢氧化钠溶液反应;
C.溴腐蚀橡胶塞;
D.可用250mL容量瓶配制体积略小的溶液.
解答:
解:A.蒸馏时,温度计用于测量馏分的温度,温度计水银球应位于蒸馏烧瓶的支管口附近,故A错误;
B.氯气和氢氧化钠溶液反应,应用饱和食盐水除杂,故B错误;
C.溴具有强氧化性和腐蚀性,应用玻璃塞,故C错误;
D.可用250mL容量瓶配制体积略小的溶液,避免浪费,故D正确.
故选D.
B.氯气和氢氧化钠溶液反应,应用饱和食盐水除杂,故B错误;
C.溴具有强氧化性和腐蚀性,应用玻璃塞,故C错误;
D.可用250mL容量瓶配制体积略小的溶液,避免浪费,故D正确.
故选D.
点评:本题考查较为综合,涉及气体的除杂、分离,药品的存放以及溶液的配制,综合考查学生的分析能力、实验能力和评价能力,为高考常见题型,注意把握物质的性质的异同以及实验的严密性和可行性的评价,难度不大.

练习册系列答案
相关题目
下列实验设计及其对应的离子方程式均正确的是( )
| A、Ca(C1O)2溶液中通入少量SO2气体:Ca2++2C1O-+SO2+H2O=CaSO3↓+2HC1O |
| B、澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-=CaCO3↓+H2O |
| C、向硅酸钠溶液中通入过量的CO2:SiO32-+CO2+H2O=H2SiO3↓+CO32 |
| D、用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO_-+6H++5H2O2=2Mn2++5O2↑+8H2O |
同温同压下,下列有关等质量SO2和CO2的叙述中正确的是( )
| A、分子数之比1:1 |
| B、密度之比16:11 |
| C、密度之比11:16 |
| D、体积之比16:11 |
| 原子 | N | S | O | Si |
| 半径/nm | 0.075 | 0.102 | 0.074 | 0.117 |
| A、0.080 nm |
| B、0.110 nm |
| C、0.120 nm |
| D、0.070 nm |
常温常压下,某50mL三种气态烃和足量O2混合后点燃,恢复到原来的状况,体积共缩小100mL,则该混合烃可能是( )
| A、CH4、C2H2、C2H4 |
| B、C2H6、C3H6、C4H6 |
| C、CH4、C3H8、C2H6 |
| D、C2H2、C2H4、C2H6 |
膦又称磷化氢,化学式为PH3,在常温下是一种无色有大蒜气味的有毒气体,它的分子呈三角锥形.以下关于
PH3的叙述中正确的是( )
PH3的叙述中正确的是( )
| A、PH3是非极性分子 |
| B、PH3中有未成键电子对 |
| C、PH3是一种强氧化剂 |
| D、PH3分子中P-H键是非极性键 |
下列与有机物结构、性质相关的叙述错误的是( )
| A、用溴水即可鉴别苯酚溶液、2,4-已二烯和甲苯 |
| B、苯酚分子中含有羟基,可与Na2CO3溶液反应生成CO2 |
| C、甲烷和氯气反应生成一氯甲烷,与苯和硝酸反应生成硝基苯的反应类型相同 |
| D、苯不能使溴的四氯化碳溶液褪色,说明苯分子中没有与乙烯分子中类似的碳碳双键 |
在同温同压下,下列各组热化学方程式中Q2>Q1的是( )
| A、2H2(g)+O2(g)=2H2O(l)△H═-Q1 2H2(g)+O2(g)=2H2O(g)△H═-Q2 | ||||
| B、S(g)+O2(g)=SO2(g)△H═-Q1 S(s)+O2(g)=SO2(g)△H═-Q2 | ||||
C、C(s)+
| ||||
D、H2(g)+Cl2(g)=2HCl(g)△H═-Q1
|