题目内容
氯气是一种重要的工业原料.工业上利用反应3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气,若管道漏气遇氨就会产生白烟.下列说法错误的是( )
| A、白烟的成分为NH4Cl晶体颗粒 |
| B、该反应属于复分解反应 |
| C、该反应利用了Cl2的强氧化性 |
| D、生成1molN2有6mol电子转移 |
考点:氯气的化学性质
专题:卤族元素
分析:反应3Cl2+2NH3=N2+6HCl中,Cl元素化合价降低,被还原,Cl2为氧化剂,N元素化合价升高,被氧化,NH3为还原剂,NH3可与HCl反应生成氯化铵,有白烟生成,以此解答.
解答:
解:A.反应生成HCl,NH3可与HCl反应生成氯化铵,有白烟生成,故A正确;
B.反应中Cl和N元素化合价发生变化,属于氧化还原型的置换反应,故B错误;
C.Cl元素化合价降低,被还原,Cl2为氧化剂,故C正确;
D.N元素化合价由-3价升高到0价,则生成1molN2时有6mol电子转移,故D正确.
故选B.
B.反应中Cl和N元素化合价发生变化,属于氧化还原型的置换反应,故B错误;
C.Cl元素化合价降低,被还原,Cl2为氧化剂,故C正确;
D.N元素化合价由-3价升高到0价,则生成1molN2时有6mol电子转移,故D正确.
故选B.
点评:本题考查氯气的性质,侧重于化学与生活、生产的联系以及氧化还原反应的考查,注意从元素化合价的角度解答该题,难度不大.

练习册系列答案
相关题目
下列关于胶体的有关说法中,不正确的是( )
| A、用丁达尔效应可以鉴别氯化铁溶液和氢氧化铁胶体 |
| B、明矾能净水,是因为溶于水能形成胶体,吸附性强 |
| C、胶体静置片刻后会出现分层现象 |
| D、胶体、溶液和浊液的本质区别是分散质粒子的大小不同 |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、物质的量浓度为1 mol/L的K2SO4溶液中,含2 NA个K+ |
| B、把40 g NaOH固体溶于1 L水中,所得溶液中NaOH的物质的量浓度为1 mol?L-1 |
| C、常温常压下,71 g Cl2含有2 NA个Cl原子 |
| D、标准状况下,11.2 L 氦气中含有的原子数为NA |
下列说法或表示方法正确的是( )
| A、乙烯的结构简式:CH2CH2 |
B、一CH3(甲基)的电子式: |
C、硝基苯的结构简式: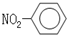 |
D、聚乙烯的结构简式为: |
一定有化学变化发生的过程是( )
| A、蒸馏 | B、升华 | C、燃烧 | D、蒸发 |
现有下列短周期元素性质的数据:下列说法正确的是( )
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径 | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
| A、原子序数④元素小于⑦元素 |
| B、上述八种元素最高价氧化物对应的水化物,⑤号酸性最强 |
C、⑧号元素离子结构示意图为: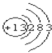 |
| D、②、③处于同一周期 |