题目内容
磷酸燃料电池是目前较为成熟的燃料电池,其基本组成和反应原理如下.

(1)在改质器中主要发生的反应为
(2)移位反应器中CO(g)+H2O (g)?CO2 (g)+H2(g),在一定温度下,在1L容器中发生上述反应,各物质的物质的量浓度变化如下表:
①此温度下,该反应的平衡常数为
②反应在3~4min之间,氢气的物质的量增多的原因可能是 (填代号)
A.充入水蒸汽 B.升高温度 C.使用催化剂 D.充入氢气
(3)磷酸燃料电池负极排出的气体主要是 ,该电池正极的电极反应为 .
(4)磷酸燃料电池的电极上镀了铂粉,这样做的目的,除了起到更好的导电作用外,还具备的作用是 .
(5)总体看来,整个体系中能量来自与CxHy与空气的反应,假设CxHy为辛烷,且已知辛烷的燃烧热为5 518kJ?mol-1,请写出辛烷燃烧热的热化学方程式 .

(1)在改质器中主要发生的反应为
(2)移位反应器中CO(g)+H2O (g)?CO2 (g)+H2(g),在一定温度下,在1L容器中发生上述反应,各物质的物质的量浓度变化如下表:
| t/min | COmol/L) | H2O(mol/L) | CO2(mol/L) | H2(mol/L) |
| 0 | 0.2 | 0.3 | 0 | 0 |
| 2 | n1 | n2 | n3 | 0.1 |
| 3 | n1 | n2 | n3 | 0.1 |
| 4 | 0.09 | 0.19 | 0.11 | 0.11 |
②反应在3~4min之间,氢气的物质的量增多的原因可能是
A.充入水蒸汽 B.升高温度 C.使用催化剂 D.充入氢气
(3)磷酸燃料电池负极排出的气体主要是
(4)磷酸燃料电池的电极上镀了铂粉,这样做的目的,除了起到更好的导电作用外,还具备的作用是
(5)总体看来,整个体系中能量来自与CxHy与空气的反应,假设CxHy为辛烷,且已知辛烷的燃烧热为5 518kJ?mol-1,请写出辛烷燃烧热的热化学方程式
考点:化学电源新型电池,热化学方程式,化学平衡的计算
专题:基本概念与基本理论
分析:(1)根据改质器中的反应物和生成物判断反应方程式;
(2)①根据反应方程式和平衡浓度,计算平衡常数;
②根据4分钟时平衡浓度计算平衡常数,与原平衡常数比较;
(3)根据负极上废气的成分判断;正极上氧气得电子发生还原反应,注意结合电解质溶液的酸碱性书写电极反应式;
(4)增大反应物的接触面积可以加快反应速率;
(5)已知辛烷的燃烧热为5 518kJ?mol-1,结合热化学方程式书写方法标注物质聚集状态和对应焓变写出.
(2)①根据反应方程式和平衡浓度,计算平衡常数;
②根据4分钟时平衡浓度计算平衡常数,与原平衡常数比较;
(3)根据负极上废气的成分判断;正极上氧气得电子发生还原反应,注意结合电解质溶液的酸碱性书写电极反应式;
(4)增大反应物的接触面积可以加快反应速率;
(5)已知辛烷的燃烧热为5 518kJ?mol-1,结合热化学方程式书写方法标注物质聚集状态和对应焓变写出.
解答:
解:(1)改质器中进入的物质是烃和水,反应温度是800℃,出来的气体是水、氢气和一氧化碳,所以发生的化学反应是CxHy+xH2O
xCO+(x+
)H2,
故答案为:CxHy+xH2O
xCO+(x+
)H2;
(2)①CO(g)+H2O (g)?CO2 (g)+H2(g),
起始浓度(mol/L):0.2 0.3 0 0
转化浓度(mol/L):0.1 0.1 0.1 0.1
平衡浓度(mol/L):0.1 0.2 0.1 0.1
则K=
=
=0.5;
故答案为:0.5;
②4分钟时平衡浓度:c(CO)=0.09mol/L,c(H2O)=0.19mol/L,c(CO2)=0.11mol/L,c(H2)=0.11mol/L,
则K=
=
=0.71,4分钟时平衡常数比原平衡常数大,则平衡正移,
A.充入水蒸汽,平衡常数不变,故A错误;
B.升高温度,平衡常数改变,故B正确;
C.使用催化剂,平衡常数不变,故C错误;
D.充入氢气,平衡常数不变,故D错误;
故答案为:B;
(3)燃料电池中,负极上燃料失去电子发生氧化反应,二氧化碳是废气,所以排出的气体是二氧化碳;燃料电池中,正极上氧化剂得电子和氢离子反应生成水,电极反应式为O2+4H++4e-=2H2O;
故答案为:CO2;O2+4H++4e-=2H2O;
(4)磷酸燃料电池的电极上镀了铂粉,电极表面积增大,能增大电极单位面积吸附H2、O2分子数,加快反应速率;
故答案为:增大电极单位面积吸附H2、O2分子数,加快反应速率;
(5)已知辛烷的燃烧热为5 518kJ?mol-1,则25℃、101kpa下,1molC8H18(辛烷)燃烧生成二氧化碳和液态水时放出5 518kJ热量,所以反应的热化学方程式为:C8H18(l)+
O2(g)═8CO2(g)+9H2O(l)△H=-5 518kJ?mol-1,
故答案为:C8H18(l)+
O2(g)═8CO2(g)+9H2O(l)△H=-5 518kJ?mol-1.
| 高温 |
| y |
| 2 |
故答案为:CxHy+xH2O
| 高温 |
| y |
| 2 |
(2)①CO(g)+H2O (g)?CO2 (g)+H2(g),
起始浓度(mol/L):0.2 0.3 0 0
转化浓度(mol/L):0.1 0.1 0.1 0.1
平衡浓度(mol/L):0.1 0.2 0.1 0.1
则K=
| c(H2)?c(CO2) |
| c(CO)?c(H2O) |
| 0.1×0.1 |
| 0.1×0.2 |
故答案为:0.5;
②4分钟时平衡浓度:c(CO)=0.09mol/L,c(H2O)=0.19mol/L,c(CO2)=0.11mol/L,c(H2)=0.11mol/L,
则K=
| c(H2)?c(CO2) |
| c(CO)?c(H2O) |
| 0.11×0.11 |
| 0.19×0.09 |
A.充入水蒸汽,平衡常数不变,故A错误;
B.升高温度,平衡常数改变,故B正确;
C.使用催化剂,平衡常数不变,故C错误;
D.充入氢气,平衡常数不变,故D错误;
故答案为:B;
(3)燃料电池中,负极上燃料失去电子发生氧化反应,二氧化碳是废气,所以排出的气体是二氧化碳;燃料电池中,正极上氧化剂得电子和氢离子反应生成水,电极反应式为O2+4H++4e-=2H2O;
故答案为:CO2;O2+4H++4e-=2H2O;
(4)磷酸燃料电池的电极上镀了铂粉,电极表面积增大,能增大电极单位面积吸附H2、O2分子数,加快反应速率;
故答案为:增大电极单位面积吸附H2、O2分子数,加快反应速率;
(5)已知辛烷的燃烧热为5 518kJ?mol-1,则25℃、101kpa下,1molC8H18(辛烷)燃烧生成二氧化碳和液态水时放出5 518kJ热量,所以反应的热化学方程式为:C8H18(l)+
| 25 |
| 2 |
故答案为:C8H18(l)+
| 25 |
| 2 |
点评:本题考查了燃料电池原理、化学平衡的有关计算、热化学方程式的书写等知识点,题目难度中等,注意电极反应式的书写要结合电解质溶液的酸碱性,把握三段式在化学平衡计算中的应用.

练习册系列答案
相关题目
用惰性电极电解下列溶液,一段时间后,停止电解,向溶液中加入一定质量的另一种物质(括号内),能使溶液完全复原的是( )
| A、CuCl2 (CuO) |
| B、NaOH (NaOH) |
| C、CuSO4 (CuCO3) |
| D、NaCl (NaOH) |
关于用CCl4萃取碘水的 说法中不正确的是( )
| A、碘在CCl4中的溶解度大于在水中的溶解度 |
| B、萃取后水层颜色变浅 |
| C、萃取后CCl4溶液层为紫红色 |
| D、萃取后水层颜色变红且在下层 |
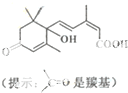 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )| A、1 mol S-诱抗素的分子能与2molNaOH反应 |
| B、能发生加成、取代、消去反应 |
| C、S-诱抗素的分子式为C14H19O4 |
| D、含有碳碳双键、苯环、羟基、羰基、羧基 |
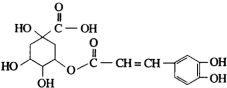 金银花有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法正确的是( )
金银花有效活性成分为绿原酸,又名咖啡鞣酸,具有广泛的杀菌消炎功效,结构如图所示,下列有关绿原酸的说法正确的是( )| A、绿原酸的分子式为C16H8O9 |
| B、1mol绿原酸最多与7molNaOH反应 |
| C、1个绿原酸分子中含有4个手性碳原子 |
| D、绿原酸分子中有4种化学环境不同的氢原子 |
在无色溶液中能大量共存的离子组是( )
| A、Cu2+、SO42-、Ba2+、Cl- |
| B、Ca2+、Na+、NO3-、CO32- |
| C、Cl-、H+、Na+、CO32- |
| D、Na+、NO3-、K+、SO42- |
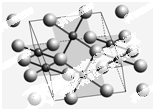 开发新型储氢材料是氢能利用的重要研究方向.
开发新型储氢材料是氢能利用的重要研究方向.