题目内容
20.下列各项叙述中正确的是( )| A. | 在同一个电子层上运动的电子,其自旋方向肯定不同 | |
| B. | 杂化轨道可用于形成σ键、π键或用于容纳未参与成键的孤电子对 | |
| C. | 物质的键能越大,该物质本身具有的能量越低 | |
| D. | 在周期表中原子的族序数等于它的最外层电子数 |
分析 A、同一电子层上运动的电子,其自旋方向有可能相同,如2p能级只容纳2个电子,自旋方向相同;
B、杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子,不能形成π键;
C、根据化学键键能越小,越容易断裂,则物质越不稳定来分析;
D、原子结构中,最外层电子数=主族序数.
解答 解:A、同一原子轨道上运动的两个电子,自旋方向肯定不同;但同一电子层上运动的电子,其自旋方向有可能相同,如2p能级只容纳2个电子,自旋方向相同,故A错误;
B、杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子,不能形成π键,π键是肩并肩形成的,故B错误;
C、化学键键能越大,越难断裂,则物质能量越低,越稳定,故C正确;
D、原子结构中,最外层电子数=主族序数,则主族元素原子最外层电子数等于族序数,故D错误;
故选C.
点评 本题考查杂化轨道和杂化理解,侧重考查对基本概念、基本理论的理解,知道原子杂化方式的判断方法,为高考热点,题目难度中等.

练习册系列答案
相关题目
8.在某温度下,可逆反应mA(g)+nB(g)?pC(g)+qD(g)的平衡常数为K,下列说法正确的是( )
| A. | K越大,达到平衡时,反应进行的程度越大 | |
| B. | K随反应物浓度的改变而改变 | |
| C. | K越小,达到平衡时,反应物的转化率越大 | |
| D. | K随温度和压强的改变而改变 |
15.根据元素周期表和元素周期律,下列推断中错误的是( )
| A. | 砹是一种有色固体,它的气态氢化物很不稳定 | |
| B. | F2与水反应比Cl2与水反应剧烈 | |
| C. | 铷的最高价氧化物的水化物一定是强碱 | |
| D. | 由Cl元素和S元素的最低化合价分别为-1和-2,推知元素的非金属性S>Cl |
12.向NaOH溶液中缓慢通入CO2气体,溶液中CO32-的物质的量与通入CO2物质的量的关系图如下.下列关于图中a、b两点溶液的说法错误的是( )


| A. | a、b两点溶液中水的电离程度相同 | |
| B. | a、b两点溶液的pH满足:pH(a)>pH(b) | |
| C. | c点溶液满足:c(Na+)>c(CO3 2-)>c(OH-)>c(HCO3-)>c(H+) | |
| D. | a、b、c三点溶液都满足:c(Na+)+c(H+)=c(HCO3-)+2c(CO3 2-)+c(OH-) |
9.某溶液中含H+、SO42-、NO3-三种离子,其中H+、SO42-的物质的量浓度分别为7.0mol•L-1和2.0mol•L-1.取该溶液20mL,加入3.2g铜粉,加热使它们充分反应,产生的气体在标准状况下的体积约为( )
| A. | 0.75 L | B. | 0.336 L | C. | 1.5 L | D. | 0.448 L |
10.室温下,0.1mol•L-1NaHCO3溶液的pH=8.31,有关该溶液的判断正确的是( )
| A. | c(Na+)>c(OH-)>c(HCO3-)>c(CO32-)>c(H+) | |
| B. | Ka1(H2CO3)•Ka2(H2CO3)<KW | |
| C. | c(H+)+c(Na+)=c(OH-)+c(HCO3-)+c(CO32-) | |
| D. | 加入适量NaOH溶液后:c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-) |
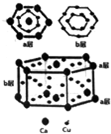 短周期元素A、B、C、D、E的原子序数依次增大,且原子最外层电子数之和为17.A是元素周期表中原子半径最小的元素,B原子的最外层电子数是其次最外层电子数的2倍,A与E同主族,D原子核外有2个未成对电子.
短周期元素A、B、C、D、E的原子序数依次增大,且原子最外层电子数之和为17.A是元素周期表中原子半径最小的元素,B原子的最外层电子数是其次最外层电子数的2倍,A与E同主族,D原子核外有2个未成对电子.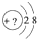 某同学在画某种元素的一种单核微粒的结构的示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断.
某同学在画某种元素的一种单核微粒的结构的示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断. .
.