题目内容
9.下列分子或离子在指定的分散系中能大量共存的一组是( )| A. | 无色溶液:K+、Cu2+、NO3-、AlO2- | |
| B. | 空气:CH4、CO2、SO2、NO | |
| C. | 氢氧化铁胶体:H+、K+、S2-、Br - | |
| D. | 各离子物质的量浓度相等的溶液:K+、Mg2+、SO42-、NO3- |
分析 A.Cu2+为蓝色;
B.NO易被氧化;
C.胶体发生聚沉,后溶解再发生氧化还原反应;
D.离子之间不反应,且遵循电荷守恒.
解答 解:A.Cu2+为蓝色,与无色不符,且Cu2+、AlO2-发生相互促进水解反应,故A错误;
B.NO易被氧化,不能稳定存在,故B错误;
C.胶体发生聚沉,后溶解再Fe3+与S2-氧化还原反应,不能共存,故C错误;
D.离子之间不反应,可大量共存,且遵循电荷守恒,故D正确;
故选D.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重水解反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.实验室需要480mL 0.1mol•L-1硫酸铜溶液,以下操作中正确的是( )
| A. | 称取7.86g硫酸铜,加入500mL水 | |
| B. | 称取12.0gCuSO4•5H2O,配制480mL溶液 | |
| C. | 称取8.0g硫酸铜,加入500mL水 | |
| D. | 称取12.5gCuSO4•5H2O,配制500mL溶液 |
17.已知热化学方程式:2SO2(g)+O2(g)?2SO3(g); H=-Q kJ•mol-1(Q>0).下列说法 正确的是( )
| A. | 相同条件下,2 mol SO2(g)和 1 mol O2(g)所具有的能量小于 2 mol SO3(g)所具有的能量 | |
| B. | 将 2 mol SO2(g)和 1 mol O2(g)置于一密闭容器中充分反应后,放出热量为 Q kJ | |
| C. | 增大压强或升高温度,该平衡都向逆反应方向移动 | |
| D. | 如将一定量 SO2(g)和 O2(g)置于某密闭容器中充分反应放热 Q kJ,则此过程中有 2 mol SO2(g)被氧化 |
14.下列叙述错误的是( )
| A. | 节假日燃放的五彩缤纷的烟花,和一些金属元素的焰色反应有关 | |
| B. | 硅胶常作实验室和袋装食品等的干燥剂 | |
| C. | 正常雨水的pH是5.6,酸雨的pH大于5.6 | |
| D. | 二氧化硅是现代光纤的原料 |
1.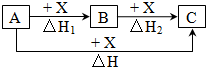 一定条件下A、B、C有如图所示的转化关系,且△H=△H1+△H2符合上述转化关系的A、C可能是①Fe、FeCl3 ②C、CO2 ③AlCl3、NaAlO2 ④NaOH、NaHCO3 ⑤S、SO3 ⑥Na2CO3、CO2( )
一定条件下A、B、C有如图所示的转化关系,且△H=△H1+△H2符合上述转化关系的A、C可能是①Fe、FeCl3 ②C、CO2 ③AlCl3、NaAlO2 ④NaOH、NaHCO3 ⑤S、SO3 ⑥Na2CO3、CO2( )
 一定条件下A、B、C有如图所示的转化关系,且△H=△H1+△H2符合上述转化关系的A、C可能是①Fe、FeCl3 ②C、CO2 ③AlCl3、NaAlO2 ④NaOH、NaHCO3 ⑤S、SO3 ⑥Na2CO3、CO2( )
一定条件下A、B、C有如图所示的转化关系,且△H=△H1+△H2符合上述转化关系的A、C可能是①Fe、FeCl3 ②C、CO2 ③AlCl3、NaAlO2 ④NaOH、NaHCO3 ⑤S、SO3 ⑥Na2CO3、CO2( )| A. | 只有②③④⑥ | B. | 除①外 | C. | 除⑤外 | D. | 全部 |
3.铜锌原电池(如图)工作时,下列叙述正确的是( )


| A. | 一段时间后铜片增重,盐桥中K+移向CuSO4溶液 | |
| B. | 正极反应为:Zn-2e-═Zn2+ | |
| C. | 电子从铜片经导线流向锌片 | |
| D. | 电池工作时Zn2+和Cu2+ 的浓度保持不变 |
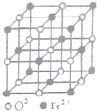 (1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、
(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、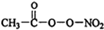 (PAN)等二次污染物.
(PAN)等二次污染物.