题目内容
短周期元素X和Y可形成离子化合物,X的阳离子与Y的阴离子相差一个电子层,下列叙述正确的是( )
| A、X和Y一定位于周期表中同一周期 |
| B、X一定是金属元素Y一定是非金属元素 |
| C、X的最高价一定比Y的最高价低 |
| D、X的原子半径一定比Y的大 |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A.该化合物可能为NaH,两种元素处于不同周期;
B.两种元素形成的化合物为离子化合物,且X形成的为阳离子、Y形成阴离子,则X为金属元素、Y为非金属元素;
C.若化合物为NaH,则两种元素的最高正价相等;
D.无论同一周期还是化合物为NaH,X的原子半径一定大于Y.
B.两种元素形成的化合物为离子化合物,且X形成的为阳离子、Y形成阴离子,则X为金属元素、Y为非金属元素;
C.若化合物为NaH,则两种元素的最高正价相等;
D.无论同一周期还是化合物为NaH,X的原子半径一定大于Y.
解答:
解:短周期元素形成离子化合物,X一定是金属元素,Y一定是非金属元素,
A.X和Y不一定位于同一周期,如NaH是离子化合物,钠和氢元素不在同一周期,故A错误;
B.二者形成的化合物为离子化合物,X形成阳离子、Y形成阴离子,则X一定是金属元素Y一定是非金属元素,故B正确;
C.X的最高价不一定比Y的最高价低,如:在NaH中,Na和H的最高价都是+1价,故C错误;
D.X和Y位于同周期时,金属半径大于非金属半径,若Y为H元素时,H原子半径最小,故D正确;
故选BD.
A.X和Y不一定位于同一周期,如NaH是离子化合物,钠和氢元素不在同一周期,故A错误;
B.二者形成的化合物为离子化合物,X形成阳离子、Y形成阴离子,则X一定是金属元素Y一定是非金属元素,故B正确;
C.X的最高价不一定比Y的最高价低,如:在NaH中,Na和H的最高价都是+1价,故C错误;
D.X和Y位于同周期时,金属半径大于非金属半径,若Y为H元素时,H原子半径最小,故D正确;
故选BD.
点评:本题考查了位置、结构与性质关系的综合应用,题目难度中等,注意掌握常见元素的原子结构、元素周期律内容、元素周期表结构,本题中注意特殊物质NaH,为易错点.

练习册系列答案
相关题目
下列溶液中微粒浓度关系一定正确的是( )
| A、将水加热到120℃,pH=6:c(OH-)<c(H+) |
| B、醋酸与醋酸钠的pH=7的混合溶液中:c(CH3COO-)>c(Na+) |
| C、0.lmoI?L-1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+) |
| D、pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)=c(H+) |
为除去镀在铝表面的铜镀层,可选用的试剂是( )
| A、稀HNO3 |
| B、浓HNO3 |
| C、浓H2SO4 |
| D、浓HCl |
下列各组中的两种物质反应时,其产物不因外界条件或反应物用量的不同而不同的是( )
| A、Na2O2和CO2 |
| B、Na和O2 |
| C、KOH和CO2 |
| D、C和O2 |
下列各图所示装置的气密性检查中,漏气的是( )
A、 |
B、 |
C、 |
D、 |
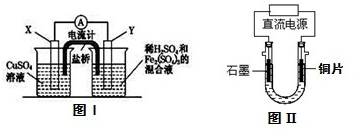 金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐.现将一定量的铜片加入到100mL稀硫酸和硫酸铁的混合溶液中,铜片完全溶解.
金属铜不溶于稀硫酸,可溶于铁盐溶液生成铜盐与亚铁盐.现将一定量的铜片加入到100mL稀硫酸和硫酸铁的混合溶液中,铜片完全溶解. 某同学想探究硫和碳原子的得电子能力的强弱,通过比较它们最高价氧化物对应水化物的酸性强弱来验证,设计了如图实验,请回答:
某同学想探究硫和碳原子的得电子能力的强弱,通过比较它们最高价氧化物对应水化物的酸性强弱来验证,设计了如图实验,请回答: