题目内容
16.有甲、乙、丙三种溶液,进行如下操作:Na2CO3溶液$\stackrel{甲}{→}$白色沉淀$\stackrel{过量乙}{→}$沉淀完全溶解并产生气体$\stackrel{丙}{→}$产生白色沉淀
则甲、乙、丙三种溶液可能是( )
| A. | BaCl2、H2SO4、MgCl2 | B. | NaCl、HNO3、AgNO3 | ||
| C. | CaCl2、HNO3、NaCl | D. | BaCl2、HCl、Na2SO4 |
分析 由Na2CO3溶液$\stackrel{甲}{→}$白色沉淀$\stackrel{过量乙}{→}$沉淀完全溶解并产生气体$\stackrel{丙}{→}$产生白色沉淀可知,白色沉淀为碳酸盐(为碳酸钡或碳酸钙等),乙为酸(盐酸、硝酸等),丙为硫酸盐,以此来解答.
解答 解:A.甲为BaCl2,乙为H2SO4,碳酸钡与硫酸反应生成硫酸钡,沉淀不能完全溶解,故A不选;
B.甲为NaCl,与碳酸钠不反应,故B不选;
C.甲为CaCl2,白色沉淀碳酸钙与HNO3生成硝酸钙,再加NaCl不反应,故C不选;
D.甲为BaCl2,乙为HCl,白色沉淀为碳酸钡,与盐酸反应生成氯化钡和二氧化碳,氯化钡再与丙(Na2SO4)反应生成BaSO4白色沉淀,故D选;
故选D.
点评 本题考查无机物的推断,为高频考点,把握物质的性质、发生的反应和现象为解答的关键,侧重分析与推断能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
6.下列物质按照混合物、非电解质、碱、酸式盐的顺序排列正确的是( )
| A. | 漂白粉、Cl2、氨水、NaHCO3 | B. | 福尔马林、苯、Cu2(OH)2CO3、明矾 | ||
| C. | 盐酸、SO2、纯碱、NH4Cl | D. | 食醋、C2H5OH、苛性钾、NaHSO4 |
4.25℃、101kPa下,1g氢气燃烧生成液态水,放出142.9kJ热量,能表示H2燃烧热的热化学方程式为( )
| A. | 2H2(g)+O2(g)═2H2O(1)△H=-571.6kJ/mol | B. | 2H2(g)+O2(g)═2H2O(1)△H=+571.6 kJ/mol | ||
| C. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-285.8 kJ/mol | D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(1)△H=-285.8kJ/mol |
11.如图所示的实验操作中,正确的是( )
| A. |  摇匀 | B. | 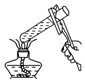 给溶液加热 | C. |  滴加液体 | D. | 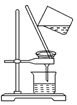 过滤 |
1.下列说法正确的是( )
| A. | 用水无法鉴别乙醇、甲苯和溴苯 | |
| B. | 可用酸性高锰酸钾溶液除去甲烷中的乙烯 | |
| C. | C2H5OOCCOOC2H5的名称:二乙酸乙二酯 | |
| D. | 除去苯中的苯酚可加入氢氧化钠溶液后分液 |
8.有甲、乙、丙三瓶等体积、等物质的量浓度的NaOH溶液,若甲不变,将乙蒸发掉一半水(溶质不析出),丙中通入一定量的CO2.然后以甲基橙作指示剂,用相同浓度的盐酸滴定,分别达到终点消耗盐酸的体积是( )
| A. | V甲=V乙>V丙 | B. | V丙>V乙>V甲 | C. | V乙>V丙>V甲 | D. | V甲=V乙=V丙 |
5.在盛放酒精的试剂瓶标签上应印有下列警示标记中的( )
| A. |  | B. |  | C. |  | D. |  |
 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.