题目内容
1.海水是巨大的资源宝库,利用海水提取一些重要的化工产品的工艺流程如图所示,回答下列问题: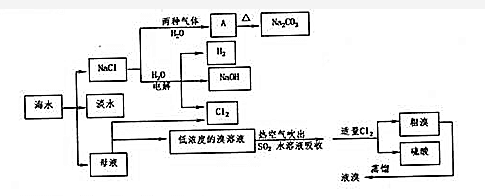
(1)请列举海水变为淡水的三种方法蒸馏法;离子交换法、电渗析法.
(2)海水晒盐得到的粗盐中含Ca2+、Mg2+、SO42-等杂质,精制过程中除去三种离子加入试剂的顺序为NaOH、BaCl2 、Na2CO3(试剂为:Na2CO3、NaOH、BaCl2),其中除去Mg2+所发生反应的离子方程式为Mg2++2OH-=Mg(OH)2↓,之后过滤(填操作名称),再加入适量盐酸,将所得溶液蒸发结晶,得到精盐.
(3)由NaCl制取A通入的两种气体的先后顺序为NH3、CO2(填化学式),写出反应的化学方程式CO2+NH3+NaCl+H2O=NaHCO3↓+NH4Cl.
(4)在蒸馏过程中,溴出口温度要控制在80~90℃,温度过高或锅底均不利于生产,理由是温度过高,大量水蒸气随之排出,溴气中水分增加;温度过低,溴不能完全蒸出,产率低.
(5)若用二甲醚(CH3OCH3)碱性燃料电池电解饱和NaCl溶液,电池的负极反应式为CH3OCH3-12e-+3H2O=2CO2+12H+;理论上,当电解槽中每小时通过1A的直流电可以产生1.492g的烧碱,某工程用290个电解槽串联生产8小时,制得30%的烧碱溶液113m3(密度为1.342t•m-3).电解槽的电流前度为1.45×104A,该电解槽的电解效率为90.6%(电解效率=$\frac{通过电解槽的电流强度}{电解槽的电流强度}$×100%,保留3位有效数字)
分析 (1)淡化海水,应降低水中的离子浓度,可用蒸馏法、离子交换法、电渗析法等;
(2)粗盐中含少量Ca2+、Mg2+、SO42-和泥沙等杂质,粗盐精制的过程中涉及常规操作步骤有:
①加水溶解;②依次加入过量的BaCl2、NaOH、Na2CO3溶液;③过滤除去沉淀;④加入适量的稀盐酸除去过量的氢氧化钠和碳酸钠;⑤蒸发浓缩、冷却结晶得到精盐;
(3)生成A的方法是侯氏制碱法,在制取A的过程中需向饱和NaCl溶液中先通入NH3,后通入气体的化学式为CO2,因为NH3极易溶于水,而CO2能溶于水,先通入氨气可吸收更多的CO2,才能生成NaHCO3;
(4)在溴水中,溴的沸点是58.5°C,水的是100°C,温度80℃-90℃时,水不沸腾而溴蒸气挥发;
(5)原电池负极发生氧化反应,二甲醚在负极放电,酸性条件下生成二氧化碳,据此解答即可;依据转移电子数计算生成NaOH的质量,根据理论耗电量和实际耗电量计算得到.
解答 解:(1)常见淡化海水的方法有蒸馏法、离子交换法、电渗析法等,故答案为:蒸馏法;离子交换法、电渗析法;
(2)先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,则加入试剂顺序为NaOH,BaCl2,Na2CO3,HCl,加试剂Na2CO3后,杂质离子转化为沉淀,则应先进行一个实验操作为过滤,其中除去Mg2+所发生反应的离子方程式为:Mg2++2OH-=Mg(OH)2↓,
故答案为:NaOH,BaCl2,Na2CO3;Mg2++2OH-=Mg(OH)2↓;过滤;
(3)生成A的方法是侯氏制碱法.因为NH3极易溶于水,而CO2能溶于水,先通入氨气可吸收更多的CO2,这样才能生成NaHCO3,所以在制取NaHCO3的过程中需向饱和NaCl溶液中先通入NH3,后通入CO2,反应的化学方程式为:CO2+NH3+NaCl+H2O=NaHCO3↓+NH4Cl,
故答案为:NH3、CO2;CO2+NH3+NaCl+H2O=NaHCO3↓+NH4Cl;
(4)在溴水中,溴的沸点是58.5°C,水的是100°C,温度过高,大量水蒸气随之排出,溴气中水分增加;温度过低,溴不能完全蒸出,产率低,
故答案为:温度过高,大量水蒸气随之排出,溴气中水分增加;温度过低,溴不能完全蒸出,产率低;
(5)原电池负极发生氧化反应,二甲醚在负极放电,酸性条件下生成二氧化碳,电极反应式为:CH3OCH3-12e-+3H2O=2CO2+12H+,烧碱溶液总含氢氧化钠的实际质量为:1.342×106×113×30%=45.49×106kg;理论上生成氢氧化钠的质量为:1.492×1.45×104×290×8=50.19×106kg;
该电解槽的电解效率η(NaOH)=$\frac{45.49×1{0}^{6}kg}{50.19×1{0}^{6}kg}$×100%=90.6%;
故答案为:CH3OCH3-12e-+3H2O=2CO2+12H+;90.6%.
点评 本题考查了海水的综合利用,包括海水提镁、提溴、淡化等;化学方程式、离子方程式的书写等知识,综合性较强.

| A. | 滴入酚酞显红色的溶液:Na+、NH4+、NO3-、Cl- | |
| B. | 0.1 mol•L-1 Fe(NO3)2溶液:H+、Al3+、SO4 2-、Cl- | |
| C. | 0.1 mol•L-1氨水溶液:K+、Na+、NO3-、AlO2- | |
| D. | c(H+):c(OH-)=1012mol•L-1的溶液:Ca2+、NH4+、Cl-、HCO3- |
| A. | 平衡向正反应方向移动 | B. | m+n<p | ||
| C. | 气体A的转化率升高 | D. | C气体的体积分数增大 |
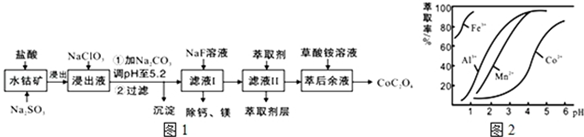
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)NaClO3的作用是将浸出液中的Fe2+氧化成Fe3+,产物中氯元素处于最低化合价.该反应的离子方程式为ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O.
(3)萃取剂对金属离子的萃取率与pH的关系如图2所示.滤液Ⅱ中加入萃取剂的作用是除去溶液中的Mn2+;使用萃取剂适宜的pH是B.
A.接近2.0 B.接近3.0 C.接近5.0
(4)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀.已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10.当加入过量NaF后,所得滤液$\frac{c(M{g}^{2+})}{c(C{a}^{2+})}$=0.7.
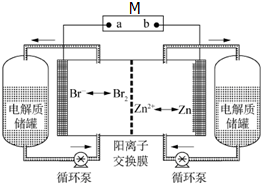 锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解质溶液在电解质储罐和电池间不断循环流动.左侧电极为惰性电极.放电时M是用电器,充电时M是外电源.下列说法不正确的是( )
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解质溶液在电解质储罐和电池间不断循环流动.左侧电极为惰性电极.放电时M是用电器,充电时M是外电源.下列说法不正确的是( )| A. | 锌溴液流电池总反应为:Zn+Br2═ZnBr2 | |
| B. | 放电时右侧电池电极发生氧化反应,电流从a极经用电器流向b极 | |
| C. | 放电时Zn2+从右侧经阳离子交换膜移向左侧,左侧电解质储罐中的离子总浓度增大 | |
| D. | 充电时左侧溴离子浓度下降,左侧电池电极连接电源的负极 |
| A. | 向该溶液中加入过量NaOH溶液,仍能大量存在:ClO-、K+、CO32-、Cl- | |
| B. | 用明矾作净水剂:Al3++3H2O=Al(OH)3↓+3H+ | |
| C. | 向该溶液中加入过量Ba(OH)2溶液,有白色沉淀生成2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| D. | 将该溶液蒸干、灼烧得到是K 2SO4和Al2O3 |
 .
. .
. .
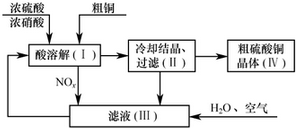
. 钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途.
钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途.