题目内容
加入铝粉能放出H2的溶液中肯定不能大量共存的离子组是( )
| A、Fe3+、NO3-、Cl-、NH4+ |
| B、Ba2+、Mg2+、HCO3-、Cl-? |
| C、SO42-、Cl-、K+、NH4+ |
| D、SO32-、K+、AlO2-、Na+ |
考点:离子共存问题
专题:离子反应专题
分析:加入铝粉能放出H2的溶液为酸性或者碱性溶液,溶液中存在大量氢离子或氢氧根离子,
A.碱性溶液中,铁离子、铵根离子与氢氧根离子反应,酸性溶液中,硝酸根离子具有强氧化性,无法生成氢气;
B.碳酸氢根离子既能够与氢离子,也能够与氢氧根离子反应;
C.在酸性条件下,SO42-、Cl-、K+、NH4+离子之间不发生反应,也不与氢离子反应;
D.在碱性溶液中,SO32-、K+、AlO2-、Na+离子之间不发生反应,也不与氢氧根离子反应.
A.碱性溶液中,铁离子、铵根离子与氢氧根离子反应,酸性溶液中,硝酸根离子具有强氧化性,无法生成氢气;
B.碳酸氢根离子既能够与氢离子,也能够与氢氧根离子反应;
C.在酸性条件下,SO42-、Cl-、K+、NH4+离子之间不发生反应,也不与氢离子反应;
D.在碱性溶液中,SO32-、K+、AlO2-、Na+离子之间不发生反应,也不与氢氧根离子反应.
解答:
解:加入铝粉能放出H2的溶液为酸性或者碱性溶液,溶液中存在大量H+或OH-,
A.碱性溶液中,Fe3+、NH4+子与氢氧根离子反应,酸性溶液中,硝酸根离子具有强氧化性,无法生成氢气,在溶液中一定不能大量共存,故A正确;
B.HCO3-既能够与氢离子,也能够与氢氧根离子反应,在溶液中一定不能大量共存,故B正确;
C.在酸性条件下,SO42-、Cl-、K+、NH4+离子之间不反应,也不与氢离子反应,在溶液中能够大量共存,故C错误;
D.在碱性溶液中,SO32-、K+、AlO2-、Na+离子之间不反应,也不与氢氧根离子反应,在溶液中可以大量共存,故D错误;
故选AB.
A.碱性溶液中,Fe3+、NH4+子与氢氧根离子反应,酸性溶液中,硝酸根离子具有强氧化性,无法生成氢气,在溶液中一定不能大量共存,故A正确;
B.HCO3-既能够与氢离子,也能够与氢氧根离子反应,在溶液中一定不能大量共存,故B正确;
C.在酸性条件下,SO42-、Cl-、K+、NH4+离子之间不反应,也不与氢离子反应,在溶液中能够大量共存,故C错误;
D.在碱性溶液中,SO32-、K+、AlO2-、Na+离子之间不反应,也不与氢氧根离子反应,在溶液中可以大量共存,故D错误;
故选AB.
点评:本题考查离子共存的正误判断,为中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;解决离子共存问题时还应该注意题目所隐含的条件,如:“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
相关题目
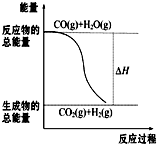 燃烧热是指一定条件下1mol可燃物完全燃烧生成稳定的氧化物时放出的热量.已知热化学方程式:①CO(g)+
燃烧热是指一定条件下1mol可燃物完全燃烧生成稳定的氧化物时放出的热量.已知热化学方程式:①CO(g)+| 1 |
| 2 |
| 1 |
| 2 |
| A、由反应①、②可知如图所示的热化学方程式为CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41.2 kJ?mol-1 | ||
| B、H2的燃烧热为241.8 kJ?mol-1 | ||
| C、H2(g)转变成H2O(g)的化学反应一定要释放能量 | ||
D、根据②推知反应H2(g)+
|
下列除杂选用的试剂和方法不完全正确的是( )
| 选项 | 被提纯物质 | 杂质 | 试剂 | 方法 |
| A | C2H6 | C2H4 | 溴水 | 洗气 |
| B | C2H4 | SO2 | KMnO4(H+) | 洗气 |
| C | 乙酸乙酯 | 乙酸 | 饱和Na2CO3溶液 | 分液 |
| D | 乙醇 | 水 | CaO | 蒸馏 |
| A、A | B、B | C、C | D、D |
2005年11月13日,中国石油吉林石化公司双苯厂一装置发生爆炸,导致严重污染.这次爆炸产生的主要污染物为硝基苯、苯和苯胺等.下列说法正确的是( )
| A、硝基苯是由苯与浓硝酸在浓硫酸作用下发生取代反应制取的 |
| B、苯可以发生取代反应也可以发生加成反应,但不可被氧化 |
| C、硝基苯有毒,密度比水小,可从水面上“捞出” |
| D、苯与硝基苯都属于芳香族化合物 |