题目内容
利用胆矾(CuSO4?5H2O)配制1000mL 0.5mol/L CuSO4溶液,假如其他操作均是准确无误的,下列情况会引起配制溶液的浓度偏高的是( )
| A、容量瓶中原有少量蒸馏水 |
| B、溶液从烧杯转移到容量瓶中后没有洗涤烧杯 |
| C、定容时观察液面俯视 |
| D、称取胆矾80g |
考点:溶液的配制
专题:实验评价题
分析:配制一定物质的量浓度的溶液过程中,能引起误差的原因主要有:称量不准确、转移不完全、读数不符合要求、操作不规范等,可以根据错误操作对c=
=
的影响进行判断.
| n |
| v |
| ||
| v |
解答:
解:A、在定容时需要用到蒸馏水,所以容量瓶中原有少量蒸馏水,对配制溶液的浓度无影响,故A错误;
B、没有洗涤烧杯,导致配制的溶液中溶质的物质的量减小,配制的溶液浓度偏低,故B错误;
C、定容时俯视刻度线,导致配制的溶液的体积偏小,浓度偏高,故C正确;
D、配制1000mL 0.5mol/LCuSO4溶液,需要CuSO4的物质的量为0.5mol/L×1L=0.5mol,需要硫酸铜晶体的质量为:250g/mol×0.5mol=125g,称量的硫酸铜晶体过少,浓度偏低,故D错误;
故选:C.
B、没有洗涤烧杯,导致配制的溶液中溶质的物质的量减小,配制的溶液浓度偏低,故B错误;
C、定容时俯视刻度线,导致配制的溶液的体积偏小,浓度偏高,故C正确;
D、配制1000mL 0.5mol/LCuSO4溶液,需要CuSO4的物质的量为0.5mol/L×1L=0.5mol,需要硫酸铜晶体的质量为:250g/mol×0.5mol=125g,称量的硫酸铜晶体过少,浓度偏低,故D错误;
故选:C.
点评:本题考查了配制一定浓度的溶液的误差分析,主要是熟练掌握常见误差的分析方法,本题难度不大.

练习册系列答案
相关题目
取pH值均等于1的盐酸和醋酸各100mL分别加水稀释到10倍后,再分别加入0.03g锌粉,在相同条件下充分反应,有关叙述正确的是( )
| A、醋酸与锌反应放出H2多 |
| B、盐酸和醋酸分别与锌反应放出的H2一样多 |
| C、醋酸与锌反应速率小 |
| D、盐酸和醋酸分别与锌反应的速率一样大 |
 一些装有化学物质的容器上常贴有危险化学品的标志.下列标志中的含义对应是( )
一些装有化学物质的容器上常贴有危险化学品的标志.下列标志中的含义对应是( )| A、自燃物品 | B、剧毒品 |
| C、爆炸品 | D、氧化剂 |
下列叙述正确的是( )
①在蒸发皿中,用酒精灯加热蒸发NaHCO3溶液,可以得到NaHCO3固体.②欲配置1.00L 1.00mol?L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中.③新制氯水、硝酸等试剂用棕色玻璃瓶盛装.④用渗析的方法提纯氢氧化铁胶体.⑤盐酸和食醋既是化合物又是酸.
①在蒸发皿中,用酒精灯加热蒸发NaHCO3溶液,可以得到NaHCO3固体.②欲配置1.00L 1.00mol?L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中.③新制氯水、硝酸等试剂用棕色玻璃瓶盛装.④用渗析的方法提纯氢氧化铁胶体.⑤盐酸和食醋既是化合物又是酸.
| A、①②③ | B、①④⑤ |
| C、③④ | D、④⑤ |
下列基本实验操作中,正确的是( )
A、 气体除杂 |
B、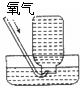 收集氧气 |
C、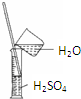 稀释溶液 |
D、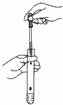 稀释溶液 |
平时实验中我们发现,同学们在进行实验时,出现许多不正确的操作方式,希望同学在今后的实验中,克服不规范的操作.请找出图示中正确的实验操作( )
A、 除去CO的CO2 |
B、 萃取时振荡混合液 |
C、 稀释浓硫酸 |
D、 向试管中滴加液体 |
重铬酸铵(NH4)2Cr2O7是一种受热易分解的盐,下列各组对重铬酸铵受热分解产物的判断,可能符合事实的是( )
①CrO3+NH3+H2O
②Cr2O3+NH3+H2O
③CrO3+N2+H2O
④Cr2O3+N2+H2O.
①CrO3+NH3+H2O
②Cr2O3+NH3+H2O
③CrO3+N2+H2O
④Cr2O3+N2+H2O.
| A、①② | B、②③ | C、①③ | D、①④ |
下面是有关厨房中的常见操作或常见现象,其中没有发生化学反应的是( )
| A、燃烧液化气为炒菜提供热量 |
| B、用洗涤精洗去锅碗上的油污 |
| C、牛奶久置变质腐败 |
| D、烧菜用过的铁锅,经放置常出现红棕色斑迹 |
下列溶液中微粒浓度关系一定正确的是( )
| A、氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+) |
| B、pH=2的一元酸和pH=12的一元强碱等体积混合:c(OH-)>c(H+) |
| C、0.1mol?L-1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| D、0.1mol?L-1的硫化钠溶液中:c(OH-)=c(H+)>c(HS-)>c(H2S) |