题目内容
15.以下是对重要金属及其化合物的讨论,根据要求回答问题:(1)金属钠在氧气中充分燃烧生成产物是淡黄色,将所得产物投入水中,产物和水迅速发生反应,写出该反应的化学方程式:2Na2O2+2H2O═4NaOH+O2↑.向上所得溶液中加入FeSO4溶液,看到的现象:生成白色沉淀,迅速变灰绿色,最后变红褐色,此过程中发生的氧化还原反应的化学方程式:4Fe(OH)2+O2+2H2O═4Fe(OH)3.
(2)铝分别与足量的NaOH溶液和稀硫酸反应,若两个反应在相同状况下放出等量的气体,则两个反应中消耗的铝的物质的量之比为1:1.
(3)向沸水中逐滴滴加1mol•L-1FeCl3溶液,至液体呈透明的红褐色,检验该红褐色的液体分散系的方法是丁达尔效应.电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板.写出该反应的离子方程式2Fe3++Cu═2Fe2++Cu2+..
分析 (1)钠在空气中燃烧生成淡黄色的过氧化钠;过氧化钠和水反应生成氢氧化钠和氧气;
过氧化钠和水反应生成氢氧化钠,氢氧化钠和亚铁离子反应生成氢氧化亚铁白色沉淀,氢氧化亚铁易被氧化生成氢氧化铁红褐色沉淀,据此写出实验现象;有电子转移的化学反应是氧化还原反应;
(2)根据转移电子守恒计算;
(3)胶体中分散质粒度介于1-100nm,检验胶体用丁达尔效应,三价铁具有强的氧化性,能够氧化铜单质.
解答 解:(1)钠在空气中燃烧生成淡黄色固体过氧化钠;过氧化钠和水反应生成氢氧化钠和氧气,反应方程式为:2Na2O2+2H2O═4NaOH+O2↑;
过氧化钠和水反应生成氢氧化钠,氢氧化钠和亚铁离子反应生成白色沉淀氢氧化亚铁,氢氧化亚铁不稳定,极易被空气中的氧气氧化而迅速变灰绿色,最后变红褐色氢氧化铁沉淀,所以实验现象是:生成白色沉淀,迅速变灰绿色,最后变红褐色,氢氧化亚铁被氧化的反应是氧化还原反应,反应方程式为:4Fe(OH)2+O2+2H2O═4Fe(OH)3.
故答案为:淡黄;2Na2O2+2H2O═4NaOH+O2↑;生成白色沉淀,迅速变灰绿色,最后变红褐色;4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(2)铝分别和足量的氢氧化钠和稀硫酸反应,如果生成相同条件下等量的氢气,这两个反应中都是铝失电子,由转移电子守恒知,需要铝的物质的量之比为1:1,故答案为:1:1;
(3)胶体中分散质粒度介于1-100nm,检验胶体用丁达尔效应,三价铁具有强的氧化性,能够氧化铜单质,所以反应的离子方程式为:2Fe3++Cu═2Fe2++Cu2+,故答案为:丁达尔效应;2Fe3++Cu═2Fe2++Cu2+.
点评 本题考查了钠的化合物的性质及氢氧化亚铁的性质等知识点,难度不大,注意:会用化学用语对实验现象进行描述,此点是高考的热点.

 名校课堂系列答案
名校课堂系列答案(1)CO可用于炼铁,已知:Fe2O3(s)+3C(s)═2Fe(s)+3CO(g)△H 1=+489.0 kJ•mol-1,
C(s)+CO2(g)═2CO(g)△H 2=+172.5 kJ•mol-1
则CO还原Fe2O3(s)的热化学方程式为Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-28.5kJmol-1.
(2)分离高炉煤气得到的CO与空气可设计成燃料电池(以KOH溶液为电解液).写出该电池的负极反应式:CO+4OH--2e-=CO32-+2H2O.
(3)CO2和H2充入一定体积的密闭容器中,在两种温度下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)测得CH3OH的物质的量随时间的变化见图1.
①曲线I、Ⅱ对应的平衡常数大小关系为KⅠ>KⅡ(填“>”或“=”或“<”).
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入
反应物,一段时间后达到平衡.
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1mol CO2、3mol H2 | a mol CO2、b mol H2 c mol CH3OH(g)、c mol H2O(g) |
(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2.紫外光照射时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,CH4产量随光照时间的变化见图2.在0~15小时内,CH4的平均生成速率Ⅰ、Ⅱ和Ⅲ从大到小的顺序为II>III>I(填序号).
(5)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸.在不同温度下催化剂的催化效率与乙酸的生成速率的关系见图3.
①乙酸的生成速率主要取决于温度影响的范围是300℃~400℃.
②Cu2Al2O4可溶于稀硝酸,写出有关的离子方程式:3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO↑+16H2O.
| A. | 三氯化铁作净水剂 | B. | 硅胶作干燥剂 | ||
| C. | 漂粉精作消毒剂 | D. | 铁粉作食品袋内的脱氧剂 |
| A. | Na+、H+、Al3+、CH3COO- | B. | Mg2+、HCO3-、Ca2+、NO3- | ||
| C. | K+、SO42-、Cl-、Cu2+ | D. | NH4+、Cl-、K+、OH- |
| A. | 化石燃料 | B. | 太阳能 | C. | 核能 | D. | 潮汐能 |
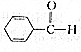 ,R的同分异构体中属于芳香化合物并能跟钠反应的种类有( )
,R的同分异构体中属于芳香化合物并能跟钠反应的种类有( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
| A. |  和 和 | B. |  与 与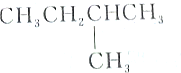 | ||
| C. |  与 与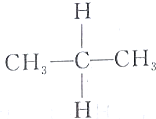 | D. |  与 与 |