题目内容
3.下列实验中不需要使用温度计的是( )| A. | 溴乙烷的水解 | B. | 苯的硝化反应 | C. | 石油的分馏 | D. | 由乙醇制乙烯 |
分析 A.溴乙烷的水解加热即可;
B.苯和浓硝酸之间发生取代反应制硝基苯,须在50-60℃下发生反应;
C.利用沸点不同,通过加热,控制蒸汽温度,分馏各组分,温度计水银球在蒸馏烧瓶支管口处;
D.乙醇和浓硫酸在170℃的条件下发生消去反应生成乙烯.
解答 解:A.溴乙烷的水解加热即可,不需要温度计,故A正确;
B.苯、浓硫酸、浓硝酸在50-60℃的水浴中反应生成硝基苯,需要温度计测量水浴的温度,故B错误;
C.石油的分馏,利用沸点不同,通过加热,控制蒸汽温度,分馏各组分,温度计水银球在蒸馏烧瓶支管口处,故C错误;
D.乙醇和浓硫酸在170℃的条件下发生消去反应生成乙烯,需要温度计测量反应液的温度,故D错误.
故选A.
点评 本题主要考查了温度计的使用,掌握常见的实验条件是解答的关键,题目难度不大.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
14.上海作为2010年世博会的举办城市,公共交通的“绿色”也已经在进行,以二甲醚(简称甲醚)为燃料的公交车作为“绿色”花园中的一点鲜艳的绿色已经正式“登台”.下列叙述正确的是( )
| A. | 甲醚作燃料会产生氮的氧化物和碳氢化合物等污染物 | |
| B. | 甲醚可由甲醇在一定条件下发生消去反应而制得 | |
| C. | 甲醚与乙醇是同分异构体 | |
| D. | 1 mol甲醚完全燃烧消耗的氧气与1 mol甲醇完全燃烧消耗的氧气相同 |
11.苹果酸的结构简式为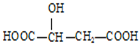 ,下列说法正确的是( )
,下列说法正确的是( )
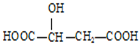 ,下列说法正确的是( )
,下列说法正确的是( )| A. | HOOC-CH2-CH(OH)-COOH与苹果酸互为同分异构体 | |
| B. | 1mol苹果酸可与3mol NaOH发生中和反应 | |
| C. | 1mol苹果酸与足量金属Na反应生成生成1mol H2 | |
| D. | 苹果酸中能发生酯化反应的官能团有2种 |
18.下列关于SiO2和CO2的说法中不正确的是( )
| A. | CO2和SiO2都能与碱及碱性氧化物反应 | |
| B. | CO2和SiO2都能与水反应生成相应的酸 | |
| C. | CO2和SiO2都能与焦炭反应生成CO | |
| D. | SiO2可用于制光导纤维,干冰可用于人工降雨 |
8.甲、乙两种非金属:能说明甲比乙的非金属性强的是( )
①甲单质比乙单质更容易与H2化合;
②甲单质能与乙的阴离子发生置换反应;
③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强;
④与某金属反应时,甲原子得电子数目比乙的多;
⑤甲的单质熔、沸点比乙的低.
①甲单质比乙单质更容易与H2化合;
②甲单质能与乙的阴离子发生置换反应;
③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强;
④与某金属反应时,甲原子得电子数目比乙的多;
⑤甲的单质熔、沸点比乙的低.
| A. | 只有④ | B. | 只有①②③ | C. | ①②③⑤ | D. | ①②③④⑤ |
15.下列说法正确的是( )
| A. | 阴阳离子间通过静电吸引形成的化学键叫做离子键 | |
| B. | HF,HCl,HBr,HI的热稳定性和酸性均依次减弱 | |
| C. | 元素非金属越强,其对应含氧酸的酸性就越强 | |
| D. | 元素周期律是元素原子核电子排布周期性变化的结果 |
12.X、Y两元素的原子,它们分别获得一个电子后,都能形成稀有气体原子的电子层结构,此过程中X放出的能量大于Y,下列推断中不正确的是( )
| A. | X的还原性大于Y | B. | X-的还原性大于Y- | ||
| C. | Y的氧化性小于X | D. | Y的氧化性大于X |
13.化学反应中旧键断裂需要( )能量.
| A. | 吸收 | B. | 放出 | C. | 不吸收也不放出 | D. | 不一定 |
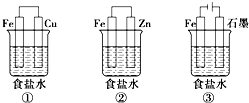 铁、铝及其化合物在生产和生活中有着广泛的应用.某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护.在相同条件下,三组装置中铁电极腐蚀最快的是①(填装置序号),该装置中正极反应式为O2+2H2O+4e-=4OH-;为防止金属Fe被腐蚀,可以采牺牲阳极的阴极保护法的是上述②(填装置序号)装置原理进行防护;装置②的负极反应的电极反应式Zn-2e-=Zn2+;装置③中总反应的离子方程式为2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+2OH-.
铁、铝及其化合物在生产和生活中有着广泛的应用.某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护.在相同条件下,三组装置中铁电极腐蚀最快的是①(填装置序号),该装置中正极反应式为O2+2H2O+4e-=4OH-;为防止金属Fe被腐蚀,可以采牺牲阳极的阴极保护法的是上述②(填装置序号)装置原理进行防护;装置②的负极反应的电极反应式Zn-2e-=Zn2+;装置③中总反应的离子方程式为2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+2OH-.