题目内容
写出下列反应的化学方程式
(1)过氧化钠与二氧化碳反应的化学方程式
(2)铁与氯气反应的化学反应方程式
(3)氯气与石灰乳反应制取漂白粉的方程式 .
(1)过氧化钠与二氧化碳反应的化学方程式
(2)铁与氯气反应的化学反应方程式
(3)氯气与石灰乳反应制取漂白粉的方程式
考点:化学方程式的书写
专题:
分析:(1)过氧化钠与二氧化碳反应生成碳酸钠和氧气;
(2)氯气具有强氧化性,铁在氯气中燃烧生成氯化铁;
(3)工业用氯气和石灰乳反应制备漂白粉,氯气和碱反应生成次氯酸钙和氯化钙和水.
(2)氯气具有强氧化性,铁在氯气中燃烧生成氯化铁;
(3)工业用氯气和石灰乳反应制备漂白粉,氯气和碱反应生成次氯酸钙和氯化钙和水.
解答:
解:(1)过氧化钠与二氧化碳反应生成碳酸钠和氧气,方程式为:2Na2O2+2CO2=2Na2CO3+O2,
故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(2)氯气能将金属氧化为最高价,铁在氯气中燃烧的产物是氯化铁,反应为:2Fe+3Cl2
2FeCl3,
故答案为:2Fe+3Cl2
2FeCl3;
(3)氯气通入石灰乳[Ca(OH)2]制取漂白粉,反应生成CaCl2、Ca(ClO)2、H2O,该反应为Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O,
故答案为:Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O.
故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(2)氯气能将金属氧化为最高价,铁在氯气中燃烧的产物是氯化铁,反应为:2Fe+3Cl2
| ||
故答案为:2Fe+3Cl2
| ||
(3)氯气通入石灰乳[Ca(OH)2]制取漂白粉,反应生成CaCl2、Ca(ClO)2、H2O,该反应为Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O,
故答案为:Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O.
点评:本题考查了化学方程式的书写,题目难度不大,注意掌握反应原理和化学方程式的书写方法,该题是高考中的高频题,侧重对学生能力的培养和训练.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
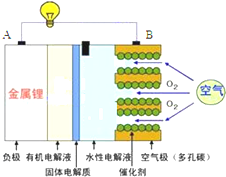 锂空气电池是一种用锂作负极,以空气中的氧气作为正极反应物的电池.其比锂离子电池具有更高的能量密度,具有很广阔的应用前景.其工作原理如图,下列说法中正确的是( )
锂空气电池是一种用锂作负极,以空气中的氧气作为正极反应物的电池.其比锂离子电池具有更高的能量密度,具有很广阔的应用前景.其工作原理如图,下列说法中正确的是( )| A、电池工作时电子从A流向B,再由B经电池内 部流向A,形成闭合回路 |
| B、电池总反应为4Li+O2=2Li2O(Li2O不溶于水) |
| C、该电池只需更换负极材料和水性电解液,可以长期供电 |
| D、用该电池电解精炼铜,理论上消耗7g锂,可以得到64g铜 |
nmolN2和nmol14CO(相对分子质量为30)相比较,下列叙述中正确的是( )
| A、二者的体积相等 |
| B、在同温同压下密度相等 |
| C、在标准情况下质量相等 |
| D、二者的分子数相等 |
对于反应aA+bB=dD+eE,若已知40g A可恰好与21g B完全反应生成28g D,则B与E的摩尔质量比为( )
| A、7a:10d |
| B、10a:7d |
| C、10b:7e |
| D、7e:11b |
警察常从案发现场的人体气味来获取有用线索,人体气味的成分中含有以下化合物:①辛酸;②壬酸;③环十二醇;④5,9?十一烷酸内酯;⑤十八烷;⑥己醛;⑦庚醛.下列说法正确的是( )
| A、①、②、⑥、⑦分子中碳原子数小于10 |
| B、①、②是无机物,③、⑤、⑦是有机物 |
| C、①是酸性化合物,②不是酸性化合物 |
| D、②、③、④含氧元素,⑤、⑥、⑦不含氧元素 |
分类思想是学习化学的重要思想,从分类的角度分析正确的是( )
| A、SO2和NO2溶于水都显酸性,因而它们都是酸性氧化物 |
| B、Na2O和NH3的水溶液均能导电,故均为电解质 |
| C、Si和SiO2均属于原子晶体 |
| D、Na2O和Na2O2与水反应均会生成强碱,故都是碱性氧化物 |
在制水泥、制玻璃、炼铁三种工业生产中,都需要的原料是( )
| A、纯碱 | B、石灰石 |
| C、粘土 | D、生石灰 |
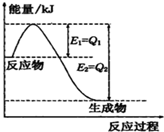 ①一定条件下,N2和H2反应生成lmolNH3过程中能量变化如图所示,则1mol N2完全反应时的焓变为:
①一定条件下,N2和H2反应生成lmolNH3过程中能量变化如图所示,则1mol N2完全反应时的焓变为: