题目内容
5.用NA表示阿伏伽德罗常数的值.下列说法中,正确的是( )| A. | 通常状况下,1molCCl4含有的分子数为NA个 | |
| B. | 0.5mol/LNH4Cl溶液中NH4+的数目小于0.2NA个 | |
| C. | 16.0gCuS和CuO的混合物中含有的铜原子数为0.3NA | |
| D. | 向FeI2溶液中通过适量氯气,当有1molFe2+被氧化时,总共转移电子的数目为NA个 |
分析 A、分子个数N=nNA;
B、溶液体积不明确;
C、Cu2S的摩尔质量是CuO的2倍,含有的铜原子也是CuO的2倍;
D、碘离子的还原性强于Fe2+.
解答 解:A、1mol四氯化碳中的分子个数N=nNA=1mol×NA/mol=NA个,故A正确;
B、溶液体积不明确,故溶液中的铵根离子的个数无法计算,故B错误;
C、Cu2S的摩尔质量是CuO的2倍,含有的铜原子也是CuO的2倍,故Cu2S和CuO的混合物可以认为是由CuO构成,则16g混合物中含有的CuO的物质的量为0.2mol,故含铜原子为0.2NA个,故C错误;
D、碘离子的还原性强于Fe2+,故当有1mol亚铁离子被氧化时,溶液中的碘离子已完全被氧化,而由于碘离子的物质的量未知,故转移的电子数无法计算,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案
相关题目
13.下列各组元素性质递变情况错误的是( )
| A. | Li、Be、B原子最外层电子数依次增多 | |
| B. | N、O、F元素最高正化合价依次升高 | |
| C. | P、S、Cl原子半径依次增大 | |
| D. | Na、K、Rb的第一电离能依次减小 |
20.已知4NH3+5O2=4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O) 表示,则正确的关系是( )
| A. | 4 v(NH3)=5 v(O2) | B. | 5 v(O2)=6 v(H2O) | C. | 4 v(O2)=5 v(NO) | D. | 2 v(NH3)=3 v(H2O) |
17.对于某些离子的检验及结论一定正确的是( )
| A. | 加入稀盐酸产生气体,将气体通入澄清石灰水,溶液变浑浊,一定有CO32- | |
| B. | 加入足量稀硝酸无明显现象,再加硝酸银溶液产生白色沉淀,一定有Cl- | |
| C. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| D. | 加入氯水,再加KSCN溶液显红色,一定有Fe3+ |
14.能使KMnO4酸性溶液褪色的物质是( )
| A. | 苯 | B. | 乙烷 | C. | 乙烯 | D. | 甲烷 |
15.用NA表示阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 1mol乙基(-CH2CH3)中含有共价键的总数为7NA | |
| B. | 1L 0.1mol/L盐酸溶液所含HCl的分子数为NA | |
| C. | 标准状况下,11.2L NO2气体中含有的分子数为0.5NA | |
| D. | 标况下11.2L CO和CO2混合气体中,所含碳原子数为0.5NA |


 ,Na2O2的电子式
,Na2O2的电子式
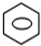 +HNO3(浓)$→_{△}^{浓硫酸}$
+HNO3(浓)$→_{△}^{浓硫酸}$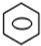 -NO2+H2O
-NO2+H2O ;
;