题目内容
2.A、B、C、D、E五种短周期元素,其原子序数逐渐增大.元素A的单质是密度最小的气体,元素B的单质存在两种以上同素异形体,且其中一种是自然界中硬度最大的单质,元素D的最外层电子数是次外层电子数的三倍.B、C、D、E四种元素均能与A形成电子数相等的四种分子,且化合物中各原子的个数比如下表:| 化合物 | 甲 | 乙 | 丙 | 丁 |
| 原子个数比 | B:A=1:3 | C:A=1:2 | D:A=1:1 | E:A=1:1 |
| A. | 元素E在元素周期表中的位置为第二周期第ⅦA族 | |
| B. | 原子半径:A<B<C<D | |
| C. | A、C、E中三种元素或任意两种元素形成的物质中只可能含有共价键 | |
| D. | A、B、C、D四元素中的三种能形成多种与甲分子电子数相等的化合物 |
分析 A、B、C、D、E五种短周期元素,其原子序数逐渐增大,元素A的单质是密度最小的气体,则A为H元素;元素B的单质存在两种以上同位素异形体,且其中一种是自然界中硬度最大的单质,则B为碳元素;元素D的最外层电子数是次外层电子数的三倍,原子只能有2个电子层,最外层电子数为6,故D为O元素;C的原子序数介于碳、氧之间,故C为N元素;B、C、D、E四种元素均能与A形成等电子数的四种分子,结合化合物中各原子的个数比,可知甲为C2H6,乙为N2H4,丙为H2O2,可推知E为Cl,丁为HCl,据此解答.
解答 解:A、B、C、D、E五种短周期元素,其原子序数逐渐增大,元素A的单质是密度最小的气体,则A为H元素;元素B的单质存在两种以上同位素异形体,且其中一种是自然界中硬度最大的单质,则B为碳元素;元素D的最外层电子数是次外层电子数的三倍,原子只能有2个电子层,最外层电子数为6,故D为O元素;C的原子序数介于碳、氧之间,故C为N元素;B、C、D、E四种元素均能与A形成等电子数的四种分子,结合化合物中各原子的个数比,可知甲为C2H6,乙为N2H4,丙为H2O2,可推知E为Cl,丁为HCl.
A.元素E为Cl,在元素周期表中的位置为第三周期第ⅦA族,故A错误;
B.同周期自左而右原子半径减小,所有元素中H原子半径最小,故原子半径H<O<N<C,故B错误;
C.H、N、Cl三种元素组成的NH4Cl含有离子键、共价键,故C错误;
D.H、C、N、O四种元素中的三种能形成CH3OH、NH2OH、CH3NH2等,与甲分子等电子数,故D正确,
故选:D.
点评 本题考查元素化合物推断,推断元素是解题关键,D选项中注意利用替换法书写18电子微粒,难度中等.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
12.25℃时,在l0mL浓度均为0.1mol.L-1的HC1和CH3COOH混合溶液中滴加0.1mol.L -1NaOH,下列有关溶液中粒子浓度关系正确的是( )
| A. | 未加NaOH时:c(H+)>c(Cl-)=c(CH3COOH) | |
| B. | 加入l0mLNaOH时:c(OH-)+c(CH3COO-)=c(H+) | |
| C. | 加入NaOH至溶液Ph=7时:c(Cl一)-c(Na+) | |
| D. | 加入20mL NaOH时:c(Na+)=c(Cl-)+c(CH3COO一') |
13.已知氧化性Br2>Fe3+.FeBr2溶液中通入一定量的Cl2,发生反应的离子方程式为:
a Fe2++b Br-+c Cl2→d Fe3++e Br2+f Cl-
下列选项中的数字与离子方程式中的a.b.c.d.e.f一一对应,其中不符合反应实际的是( )
a Fe2++b Br-+c Cl2→d Fe3++e Br2+f Cl-
下列选项中的数字与离子方程式中的a.b.c.d.e.f一一对应,其中不符合反应实际的是( )
| A. | 2 4 3 2 2 6 | B. | 0 2 1 0 1 2 | ||
| C. | 2 0 1 2 0 2 | D. | 2 2 2 2 1 4 |
17.向100mL1mol/L的AlCl3溶液中逐渐加入浓度为2mol/L的NaOH溶液,若产生3.9g白色沉淀,则加入的NaOH溶液的体积可能为( )
| A. | 30mL | B. | 55mL | C. | 65mL | D. | 175mL |
14.高铁电池是一种可逆电池,该电池能长时间保持稳定的放电电压.高铁电池总反应为3Zn+2K2Fe04+8H20?3Zn(OH)2+2Fe(OH)3+4KOH.下列判断不正确的是( )
| A. | 放电时,负极反应为2n-2e-+20H一═Zn(OH)2 | |
| B. | 充电时,阴极pH增大 | |
| C. | 放电时,若有6mol电子转移,则正极有10 mol OH一移向负极 | |
| D. | 充电时,阳极反应为Fe(OH)3+50H一+3e一=Fe042-+4H20 |
11.在热的稀H2SO4溶液中溶解了45.6g FeSO4,当加入100mL 1mol/L KNO3溶液后,使其中的Fe2+全部转化成Fe3+,KNO3也反应完全,并有NxOy气体逸出:□FeSO4+□KNO3+□H2SO4→K2SO4+□Fe2(SO4)3+□NxOy+□H2O据此推算出x、y的值分别为( )
| A. | 1、2 | B. | 1、1 | C. | 2、1 | D. | 2、3 |
12.下列事实不能用电化学理论解释的是( )
| A. | 轮船水线以下的船壳上装一定数量的锌块 | |
| B. | 银制奖牌久置后表面变暗镀锌的铁比镀锡的铁耐用 | |
| C. | 纯锌与稀硫酸反应时,滴入少量硫酸铜溶液后速率加快 | |
| D. | 镀锌的铁比镀锡的铁耐用 |
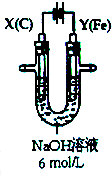 用如图所示装置进行实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.
用如图所示装置进行实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.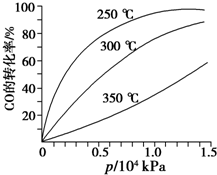 研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的处理具有重要意义.