题目内容
1.8g某物质在氯气中燃烧,质量增加了7.1g,该物质可能是( )①铁 ②铝 ③铁锂合金 ④镁铝合金.
A.只有①
B.只有②
C.②③
D.①④
【答案】分析:质量增加7.1g是参加反应的氯气的质量,氯气的物质的量为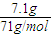 =0.1mol,假定金属都是+1价,计算的物质的量为0.2mol,则金属的摩尔质量为
=0.1mol,假定金属都是+1价,计算的物质的量为0.2mol,则金属的摩尔质量为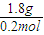 =9g/mol,据此结合平均值判断.
=9g/mol,据此结合平均值判断.
解答:解:质量增加7.1g是参加反应的氯气的质量,氯气的物质的量为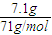 =0.1mol,假定金属都是+1价,计算的物质的量为0.2mol,则金属的摩尔质量为
=0.1mol,假定金属都是+1价,计算的物质的量为0.2mol,则金属的摩尔质量为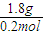 =9g/mol,
=9g/mol,
①铁与氯气反应表现+3价,假设为+1价,则其摩尔质量相当于56g/mol× =18.7g/mol,故①不符合;
=18.7g/mol,故①不符合;
②铝铁与氯气反应表现+3价,假设为+1价,则其摩尔质量相当于27g/mol× =9g/mol,故②符合;
=9g/mol,故②符合;
③铁与氯气反应表现+3价,假设为+1价,则其摩尔质量相当于56g/mol× =18.7g/mol,锂与氯气反应表现+1价,锂的摩尔质量为7g/mol,金属的平均摩尔质量9g/mol介于二者之间,故③符合;
=18.7g/mol,锂与氯气反应表现+1价,锂的摩尔质量为7g/mol,金属的平均摩尔质量9g/mol介于二者之间,故③符合;
④镁与氯气反应表现+2价,假设为+1价,则其摩尔质量相当于24g/mol× =12g/mol,铝与氯气反应表现+3价,假设为+1价,则其摩尔质量相当于27g/mol×
=12g/mol,铝与氯气反应表现+3价,假设为+1价,则其摩尔质量相当于27g/mol× =9g/mol,金属的平均摩尔质量9g/mol没有介于二者之间,故④不符合;
=9g/mol,金属的平均摩尔质量9g/mol没有介于二者之间,故④不符合;
故选C.
点评:本题考查氯气的性质、化学计算等,难度中等,利用反应进行验证比较麻烦,注意利用化合价折算确定金属的摩尔质量.
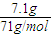 =0.1mol,假定金属都是+1价,计算的物质的量为0.2mol,则金属的摩尔质量为
=0.1mol,假定金属都是+1价,计算的物质的量为0.2mol,则金属的摩尔质量为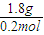 =9g/mol,据此结合平均值判断.
=9g/mol,据此结合平均值判断.解答:解:质量增加7.1g是参加反应的氯气的质量,氯气的物质的量为
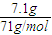 =0.1mol,假定金属都是+1价,计算的物质的量为0.2mol,则金属的摩尔质量为
=0.1mol,假定金属都是+1价,计算的物质的量为0.2mol,则金属的摩尔质量为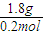 =9g/mol,
=9g/mol,①铁与氯气反应表现+3价,假设为+1价,则其摩尔质量相当于56g/mol×
 =18.7g/mol,故①不符合;
=18.7g/mol,故①不符合;②铝铁与氯气反应表现+3价,假设为+1价,则其摩尔质量相当于27g/mol×
 =9g/mol,故②符合;
=9g/mol,故②符合;③铁与氯气反应表现+3价,假设为+1价,则其摩尔质量相当于56g/mol×
 =18.7g/mol,锂与氯气反应表现+1价,锂的摩尔质量为7g/mol,金属的平均摩尔质量9g/mol介于二者之间,故③符合;
=18.7g/mol,锂与氯气反应表现+1价,锂的摩尔质量为7g/mol,金属的平均摩尔质量9g/mol介于二者之间,故③符合;④镁与氯气反应表现+2价,假设为+1价,则其摩尔质量相当于24g/mol×
 =12g/mol,铝与氯气反应表现+3价,假设为+1价,则其摩尔质量相当于27g/mol×
=12g/mol,铝与氯气反应表现+3价,假设为+1价,则其摩尔质量相当于27g/mol× =9g/mol,金属的平均摩尔质量9g/mol没有介于二者之间,故④不符合;
=9g/mol,金属的平均摩尔质量9g/mol没有介于二者之间,故④不符合;故选C.
点评:本题考查氯气的性质、化学计算等,难度中等,利用反应进行验证比较麻烦,注意利用化合价折算确定金属的摩尔质量.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
取a g某物质在氧气中燃烧,产物与过量的过氧化钠固体完全反应,测得反应后固体增重a g,则该物质不可能是
| A.H2 | B.CO | C.CH3COOH | D.C2H5OH |