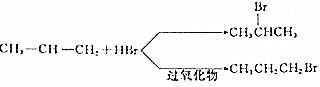
题目内容
6.X、Y、Z三种元素的离子结构都和Ar具有相同的电子层排布.H2在X单质中燃烧,产生苍白色火焰;Y元素的气态氢化物是H2Y,其最高价氧化物中Y的质量分数为40%;Z元素和氮元素在同一族.(1)根据以上条件,推断X氯,Y硫,Z磷(填写元素名称);
(2)写出它们的最高价氧化物的水化物的化学式YH2SO4,ZH3PO4.
分析 X、Y、Z三种元素的离子结构都和Ar具有相同的电子层排布,H2在X单质中燃烧,产生苍白色火焰,则X是Cl元素;
Y元素的气态氢化物是H2Y,其最高价氧化物中Y的质量分数为40%,则Y位于第VIA族,其离子结构和氩原子电子层结构相同,所以Y是S元素;
Z元素和N元素在同一族,则Z为P元素,
依据分析可知:X是Cl元素,Y是S元素,Z为P元素,再结合元素化合物知识解答.
解答 解:(1)X、Y、Z三种元素的离子结构都和Ar具有相同的电子层排布,H2在X单质中燃烧,产生苍白色火焰,则X是Cl元素;Y元素的气态氢化物是H2Y,则Y位于第VIA族,其离子结构和氩原子电子层结构相同,所以Y是S元素;Z元素和氮元素在同一族,则Z为P元素,
依据分析可知:X是Cl元素,Y是S元素,Z为P元素,
故答案为:氯;硫;磷;
(2)Y为S元素,S的最高价为+6价,S的最高价氧化物为SO3,其对应的水化物为硫酸:H2SO4;
Z为P元素,P的最高价为+5价,则P的最高价氧化物为P2O5,其对应的水化物为磷酸:H3PO4,
故答案为:H2SO4;H3PO4.
点评 本题主要考查了元素位置结构性质关系的相互应用,熟悉原子结构及物质的性质是解本题关键,根据反应现象、原子结构确定元素,再结合元素化合物的性质来分析解答.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
18.已知短周期元素的离子aA3+、bB+、cC2-、dD- 都具有相同的电子层结构,判断下列关系正确的是( )
| A. | 原子序数:a>b>d>c | B. | 原子半径:A>B>C>D | ||
| C. | 离子的还原性:D->C2- | D. | 气态氢化物的稳定性:H2C>HD |
14.分子式为C8H16O2的有机物A,它能在酸性条件下水解生成B和C,且B在一定条件下能转化成C.则有机物A的可能结构有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
1.用现代化学方法测定某有机物结构:红外光谱图表征显示有C-H键、O-H键、C-O键的振动吸收;核磁共振谱图和质谱图如下,
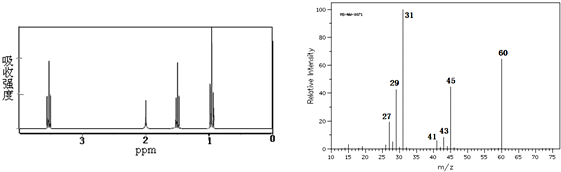
其分子结构简式为( )

其分子结构简式为( )
| A. | CH3CH2CH2OH | B. | CH3CH(OH)CH3 | C. | CH3CH2OCH3 | D. | CH3CH2CH2CHO |
11.下列叙述正确的是( )
| A. | 同温同压下,相同体积的物质,其物质的量必然相等 | |
| B. | 任何条件下,等物质的量的甲烷和一氧化碳所含的分子数必然相等 | |
| C. | 1L一氧化碳气体一定比1L氧气的质量小 | |
| D. | 同温同压下,等体积的物质所含的分子数一定相等 |
18.配制一定物质的量浓度的溶液时,由于操作不慎,转移时有些液体溅到外面,下列说法正确的是( )
| A. | 再加点溶质到容量瓶中去 | B. | 影响不大,不再处理 | ||
| C. | 重新配制 | D. | 以上措施都不正确 |
16.NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 由D和18O所组成的水11g,所含中子数为4NA | |
| B. | 1 L 0.4 mol•L-1稀硝酸与Fe完全反应,转移电子数为0.3NA | |
| C. | 标准状况下,2.24LCHCl3所含分子数为0.1NA | |
| D. | 密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA |
 、
、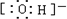 、
、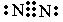 、
、 、
、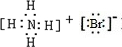 .
.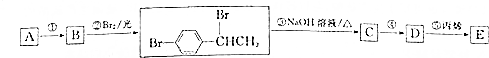
 或
或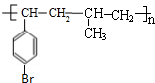 .
.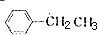 +Br2$\stackrel{铁}{→}$
+Br2$\stackrel{铁}{→}$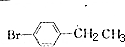 +HBr.反应③的化学方程式
+HBr.反应③的化学方程式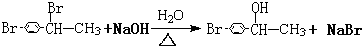 .
.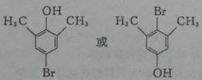 (任写一种).
(任写一种).