题目内容
已知某溶液中c(Na+)=0.2 mol/L,c(Mg2+)=0.25 mol/L,c(Cl-)=0.4 mol/L,如果溶液中还有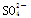 ,那么c(SO42-)应为
,那么c(SO42-)应为
A.0.1 mol/L B.0.3 mol/L C.0.15 mol/L D.0.5 mol/L
C
【解析】
试题分析:溶液中的离子遵循电荷守恒,即溶液中的阳离子带电的电荷量与阴离子所带电电荷量相等.设SO42-物质的量浓度为c,则根据电荷守恒:0.2mol/L×1+0.25mol/L×2=0.4mol×1+2c,解得c=0.15mol/L,选C。
考点:考查电荷守恒。

(14分)已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
请回答下列问题:
(1)该反应平衡常数表达式为K=______ ;ΔH___0(选填“>”、“<”或“=”)。
(2)830 ℃时,向一个5 L的密闭容器中充入0.20 mol的A和0.80 mol的B,若测得反应初始至6 S内A的平均反应速率v(A)=0.003 mol · L-1· S-1,则6 S时c(A)=______ mol·L-1;C的物质的量为______ mol 。
(3)在与(2)相同的温度、容器及A、B配比下反应经一段时间后达到平衡,此时A的转化率为______;如果这时向该密闭容器中再充入1 mol氩气,则平衡时A的转化率______ (选填“增大”、“减小”、“不变”)。
(4)判断该反应是否达到平衡的依据为______(填正确选项的字母)。
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时间改变 d.单位时间里生成C和D的物质的量相等
(5)1200 ℃时反应C(g)+D(g) A(g)+B(g)的平衡常数的值为______ 。
A(g)+B(g)的平衡常数的值为______ 。
奥运会会标是五环旗,假定奥运五环旗中的一环表示一种物质,相连环物质间一定条件下能发生常见反应,不相连环物质间不能发生反应,且四种反应中必须包含化合反应、置换反应及复分解反应,适合的一组是 ( )
| 蓝 | 黄 | 黑 | 绿 | 红 |
A | SiO2 | NaOH溶液 | CuSO4溶液 | Ag | O2 |
B | O2 | Fe | 稀H2SO4 | NaOH溶液 | CO2 |
C | O2 | NH3 | 稀H2SO4 | NaOH溶液 | Al(OH)3 |
D | Mg | Al | CO2 | Fe2O3 | KOH溶液 |