题目内容
5.已知:①2KMnO4+16HCl→2KCl+2MnCl2+5Cl2↑+8H2O②K2Cr2O7+14HCl→2KCl+2CrCl3+3Cl2↑+7H2O
③MnO2+4HCl(浓)$\stackrel{△}{→}$MnCl2+Cl2↑+2H2O
其中,KMnO4和一般浓度的盐酸反应,K2Cr2O7需和较浓的盐酸(大于6mol•L-1)反应,MnO2需和浓盐酸反应(大于8mol•L-1)反应.根据以上信息,下列叙述不正确的是( )
| A. | 上述各反应均既属于氧化还原反应,有属于离子反应 | |
| B. | 氧化性:KMnO4>K2Cr2O7>Cl2>MnO2 | |
| C. | 盐酸的浓度越大,Cl-的还原性越强 | |
| D. | 每生成1molCl2,上述各反应转移的电子数均为2NA(NA为阿伏加德罗常数的值) |
分析 A.化学反应中有元素化合价变化的属于氧化还原反应,有离子参加的化学反应是离子反应;
B.在自发进行的氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
C.盐酸的浓度越大,氯离子的还原性越强;
D.根据化合价变化判断.
解答 解:A.这三个分子中都有元素化合价变化,且都有离子参加,所以既属于氧化还原反应又属于离子反应,故A正确;
B.MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O中二氧化锰的氧化性大于氯气,故B错误;
C.盐酸的浓度越大,氯离子的浓度越大,其反应速率越快,则氯离子的还原性越强,故C正确;
D.生成1 mol Cl2转移电子数均为2[0-(-1)]NA=2 NA,故D正确
故选B.
点评 本题考查氧化还原反应,明确氧化还原反应的实质是解本题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.CuSO4是一种重要的化工原料,有关制备及性质如下所示.下列说法错误的是( )

| A. | 生成等量的CuSO4时,②消耗的酸最少,且能体现绿色化学思想 | |
| B. | 反应⑥中Y可以是葡萄糖或乙醛溶液 | |
| C. | 反应④所得混合气体X中一定有O2 | |
| D. | 反应①中H2SO4与HNO3物质的量最佳比为3:1 |
10.相同温度时,下列两个反应的反应热分别用△H1和△H2表示,则( )
①H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H1=-Q1KJ/mol
②2H2O(l)═2H2O(g)+O2(g)△H2=-Q1KJ/mol.
①H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H1=-Q1KJ/mol
②2H2O(l)═2H2O(g)+O2(g)△H2=-Q1KJ/mol.
| A. | Q1>Q2 | B. | Q1=Q2 | C. | 2Q1>Q2 | D. | Q2=Q1 |
14.将5.6L CO2 气体缓慢通过一定量的Na2O2固体,最后收集到3.36L 气体(气体体积均在标准状下测定),所得气体的质量为( )
| A. | 3.2 g | B. | 4.8 g | C. | 5.4 g | D. | 3.8 g |
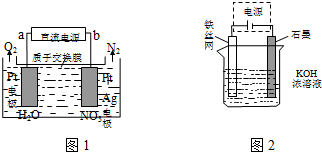
 氯碱工业中电解饱和食盐水的原理示意图如图所示:
氯碱工业中电解饱和食盐水的原理示意图如图所示: 反应A,可实现氯的循环利用。
反应A,可实现氯的循环利用。 4mol HCl被氧化,放出115.6kJ的热量。
4mol HCl被氧化,放出115.6kJ的热量。

 (一)发生在天津港“8•12”特大火灾爆炸事故,再一次引发了人们对环境问题的关注.
(一)发生在天津港“8•12”特大火灾爆炸事故,再一次引发了人们对环境问题的关注.