题目内容
4.分类法是学习和研究化学的一种常用的科学方法,下列分类合理的是( )| A. | 根据分散系的稳定性将其分为胶体、溶液和浊液 | |
| B. | 根据化合物在溶液中能否电离将其分为强电解质和弱电解质 | |
| C. | 根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸和多元酸 | |
| D. | 根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应 |
分析 A.根据分散质微粒的大小可以将混合物进行分类;
B.强电解质和弱电解质的划分是看在水中是否能够完全电离;
C.根据酸电离出的氢离子数目将酸分为一元酸、二元酸等;
D.氧化还原反应的实质是存在电子的转移.
解答 解:A.根据分散质微粒直径的大小,可以将分散系分为胶体、浊液和溶液三大类,不是依据稳定性分类,故A错误;
B.化合物在水溶液中完全电离的是强电解质,在水溶液中部分电离的属于弱电解质,故B错误;
C.根据酸电离出的氢离子数目将酸分为一元酸、二元酸等,如CH3COOH属于一元酸,故C错误;
D.氧化还原反应的实质是存在电子的转移,所以可以根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应,故D正确;
故选D.
点评 本题考查了物质的分类、氧化还原反应等,题目难度不大,物质的分类要注意分类的依据和标准,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列说法不正确的是( )
| A. | 对于相同浓度的弱酸HX和HY(前者的Ka较小)溶液,加水稀释相同倍数时,HY溶液的pH改变值大于HX溶液的pH改变值 | |
| B. | 在NH3•H2O和NH4Cl浓度均为0.1 mol•L-1的体系中,外加少量酸或碱时,溶液的pH可保持基本不变 | |
| C. | 在NaH2PO4水溶液中存在关系:c(H3PO4)+c(H+)=c(HPO42-)+c(PO43-)+c(OH-) | |
| D. | 沉淀溶解平衡AgI?Ag++I- 的平衡常数为8.5×10-17,不能说明难溶盐AgI是弱电解质 |
19.A、B、C、D均为短周期元素组成的常见物质,其中A是单质,它们之间的转化关系如图所示.
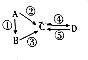
(1)若A是淡黄色固体,C是造成酸雨的物质,则符合条件的B的化学式是H2S(只写一种).1molA转化为C时,转移电子4mol.
(2)若B、D两种物质均具有两性,向反应④中通入过量的温室气体,可将C转化为D,则C与过量盐酸反应的离子方程式为AlO2-+4H+=Al3++2H2O.
(3)若A是太阳能电池用的光伏材料,B、C、D所含元素均为2种,反应①、②中的反应物除A外均含有空气中的单质,则物质D的化学式是SiF4,写出D的一种用途:有机硅化合物的合成材料.
(4)若含同种元素的物质A、B、C、D均可用于杀菌消毒、漂白,其中A是黄绿色气体,C的水溶液呈酸性,D的水溶液呈碱性.元素种类与物质之间的关系如表:
则A的电子式为 ,物质C的化学式是HClO,写出反应A→D的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O.
,物质C的化学式是HClO,写出反应A→D的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O.

(1)若A是淡黄色固体,C是造成酸雨的物质,则符合条件的B的化学式是H2S(只写一种).1molA转化为C时,转移电子4mol.
(2)若B、D两种物质均具有两性,向反应④中通入过量的温室气体,可将C转化为D,则C与过量盐酸反应的离子方程式为AlO2-+4H+=Al3++2H2O.
(3)若A是太阳能电池用的光伏材料,B、C、D所含元素均为2种,反应①、②中的反应物除A外均含有空气中的单质,则物质D的化学式是SiF4,写出D的一种用途:有机硅化合物的合成材料.
(4)若含同种元素的物质A、B、C、D均可用于杀菌消毒、漂白,其中A是黄绿色气体,C的水溶液呈酸性,D的水溶液呈碱性.元素种类与物质之间的关系如表:
| 物质 | A | B | C | D |
| 元素种类 | 1 | 2 | 3 | 3 |
 ,物质C的化学式是HClO,写出反应A→D的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O.
,物质C的化学式是HClO,写出反应A→D的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O.
14.下列反应中,SO2被还原的是( )
| A. | SO2+2NaOH=Na2SO3+H2O | B. | SO2+Cl2+2H2O=H2SO4+2HCl | ||
| C. | SO2+2H2S=3S↓+2H2O | D. | SO2+NO2=SO3+NO |

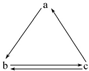 下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )