题目内容
设反应C+CO2  2CO(正反应吸热)反应速率为v1,N2+3H2
2CO(正反应吸热)反应速率为v1,N2+3H2  2NH3(正反应放热),反应速率为v2。对于上述反应,当温度升高时,v1、v2的变化情况为
2NH3(正反应放热),反应速率为v2。对于上述反应,当温度升高时,v1、v2的变化情况为
A.同时增大 B.同时减小
C.v1增大,v2减小 D.v1减小,v2增大
A
【解析】
试题分析:升高温度,加快反应速率,A正确。
考点:考查影响化学反应速率的因素。

练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
(本题共10分)水煤气转化反应CO(g)+H2O(g)  CO2(g)+H2 (g)在一定温度下达到化学平衡。完成下列填空:
CO2(g)+H2 (g)在一定温度下达到化学平衡。完成下列填空:
29.写出该反应的平衡常数表达式K=________________。
30.一定温度下,在一个容积不变的密闭容器中发生上述反应,下列说法中能判断该反应达到化学平衡状态的是 (选填编号)。
A.容器中的压强不变
B.1 mol H―H键断裂的同时断裂2 molH―O键
C.v正(CO) = v逆(H2O)
D.c(CO) = c(H2)
31.将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下实验1和实验2的数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
H2O | CO | H2 | CO | |||
1 | 650 | 2 | 4 | 1.6 | 2.4 | 3 |
2 | 650 | 1 | 2 | 0.8 | 1.2 | 5 |
3 | 950 | 1 | 2 | — | — | — |
(1)由实验组1的数据可知,平衡时CO的转化率为 %。
(2)由实验组1和2的数据可分析,压强对该可逆反应的影响是 。
(3)有了实验组1和2的数据,再设计实验3,其目的是 。

 zC(g),达平衡时,A的浓度为0.5mol/L,若保持温度不变,将容器的容积扩大到原来的两倍,达到平衡时A的浓度降为0.3mol/L。下列判断正确的是
zC(g),达平衡时,A的浓度为0.5mol/L,若保持温度不变,将容器的容积扩大到原来的两倍,达到平衡时A的浓度降为0.3mol/L。下列判断正确的是 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1 
 O2(g) == H2O(1) △H= ―285.8kJ/mol
O2(g) == H2O(1) △H= ―285.8kJ/mol
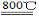 2MgCl4+Ti在Ar气氛中进行的理由是 。
2MgCl4+Ti在Ar气氛中进行的理由是 。