题目内容
硅酸钠是一种重要的无极功能材料,某研究性学习小组设计的利用海边的石英砂(含氯化钠、氧化铁等杂质)制备硅酸钠的流程如下:
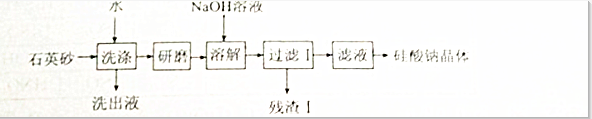
(1)石英砂加水洗涤的目的是 .研磨后加入NaOH溶液溶解的离子方程式是 .
(2)实验室进行蒸发操作要用到的仪器有铁架台(含铁圈)、 、 和 .
(3)残渣Ⅰ的成分是 (填化学式),若要检验其中的金属价态,从下列所给实际中选出合适的试剂
A.稀硫酸 B.KSCN溶液 C.氯水 D.稀硝酸
(4)硅胶可用作干燥剂,滤液中通入CO2可制得硅酸胶体,写出该反应的离子方程式: .

(1)石英砂加水洗涤的目的是
(2)实验室进行蒸发操作要用到的仪器有铁架台(含铁圈)、
(3)残渣Ⅰ的成分是
A.稀硫酸 B.KSCN溶液 C.氯水 D.稀硝酸
(4)硅胶可用作干燥剂,滤液中通入CO2可制得硅酸胶体,写出该反应的离子方程式:
考点:物质分离和提纯的方法和基本操作综合应用
专题:
分析:石英砂用水洗涤,石英砂中的氯化钠被洗涤,所以洗出液中含有NaCl,将石英砂研磨,然后加入NaOH溶液发生反应SiO2+2NaOH=Na2SiO3+H2O,然后过滤,残渣I中成分是Fe2O3,滤液中含有Na2SiO3,然后将滤液蒸发浓缩、冷却结晶得到硅酸钠;
(1)石英砂加水洗涤除去可溶性物质;二氧化硅和NaOH溶液发生反应生成硅酸钠和水;
(2)蒸发时需要的仪器有:酒精灯、铁架台、坩埚、玻璃棒;
(3)残渣I中成分是Fe2O3,三价铁离子用KSCN溶液检验;
(4)硅酸钠和二氧化碳反应生成硅酸和碳酸钠.
(1)石英砂加水洗涤除去可溶性物质;二氧化硅和NaOH溶液发生反应生成硅酸钠和水;
(2)蒸发时需要的仪器有:酒精灯、铁架台、坩埚、玻璃棒;
(3)残渣I中成分是Fe2O3,三价铁离子用KSCN溶液检验;
(4)硅酸钠和二氧化碳反应生成硅酸和碳酸钠.
解答:
解:石英砂用水洗涤,石英砂中的氯化钠被洗涤,所以洗出液中含有NaCl,将石英砂研磨,然后加入NaOH溶液发生反应SiO2+2NaOH=Na2SiO3+H2O,然后过滤,残渣I中成分是Fe2O3,滤液中含有Na2SiO3,然后将滤液蒸发浓缩、冷却结晶得到硅酸钠;
(1)石英砂加水洗涤除去可溶性物质NaCl;二氧化硅和NaOH溶液发生反应生成硅酸钠和水,离子方程式为SiO2+2OH-=SiO32-+H2O,故答案为:除去杂质NaCl;SiO2+2OH-=SiO32-+H2O;
(2)蒸发时需要的仪器有:酒精灯、铁架台、坩埚、玻璃棒,所以还需要的仪器是酒精灯、坩埚和玻璃棒,故答案为:酒精灯;坩埚;玻璃棒;
(3)通过以上分析知,残渣I中成分是Fe2O3,铁离子和KSCN溶液反应生成络合物硫氰化铁而使溶液呈血红色,三价铁离子用KSCN溶液检验,故答案为:Fe2O3;B;
(4)硅酸钠和二氧化碳反应生成硅酸和碳酸钠,离子方程式为SiO32-+CO2+H2O=H2SiO3↓+CO32-,故答案为:SiO32-+CO2+H2O=H2SiO3↓+CO32-.
(1)石英砂加水洗涤除去可溶性物质NaCl;二氧化硅和NaOH溶液发生反应生成硅酸钠和水,离子方程式为SiO2+2OH-=SiO32-+H2O,故答案为:除去杂质NaCl;SiO2+2OH-=SiO32-+H2O;
(2)蒸发时需要的仪器有:酒精灯、铁架台、坩埚、玻璃棒,所以还需要的仪器是酒精灯、坩埚和玻璃棒,故答案为:酒精灯;坩埚;玻璃棒;
(3)通过以上分析知,残渣I中成分是Fe2O3,铁离子和KSCN溶液反应生成络合物硫氰化铁而使溶液呈血红色,三价铁离子用KSCN溶液检验,故答案为:Fe2O3;B;
(4)硅酸钠和二氧化碳反应生成硅酸和碳酸钠,离子方程式为SiO32-+CO2+H2O=H2SiO3↓+CO32-,故答案为:SiO32-+CO2+H2O=H2SiO3↓+CO32-.
点评:本题考查物质分离和提纯,侧重考查实验操作、分析能力,明确各个步骤发生的反应、分离提纯方法,熟悉元素化合物性质,题目难度不大.

练习册系列答案
相关题目
常温下,pH相同的NaOH溶液和CH3COONa溶液分别加水稀释.pH随溶液体积变化的曲线如图所示,则下列叙述正确的是( )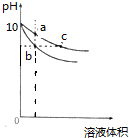

| A、b、c两点溶液的导电能力相同 |
| B、c点溶液中c (CH3COOH)+c(OH-)=c(H+) |
| C、a、b、c三点溶液中水的电离程度a>c>b |
| D、等体积的b、c两点溶液分别与相同浓度的盐酸恰好完全反应时,消耗盐酸的体积相等 |
化学科学需要借助化学专用语言描述,下列有关化学用语不正确的是( )
A、氯化钠的电子式: |
B、Cl-的结构示意图: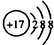 |
| C、乙烯的结构式:C2H4 |
D、CH4分子的比例模型: |
以下物质的性质只与温度有关的是( )
| A、氨气的溶解度 |
| B、水的离子积 |
| C、高锰酸钾的氧化性 |
| D、醋酸的电离度 |
在由水电离产生的c(H+)=1×10-14mol/L的溶液中,一定可以大量共存的离子组是( )
| A、K+、Ba2+、Cl-、NO3- |
| B、Na+、Ca2+、I-、NO3- |
| C、NH4+、Al3+、Br-、SO42- |
| D、K+、Na+、HCO3-、SO42- |
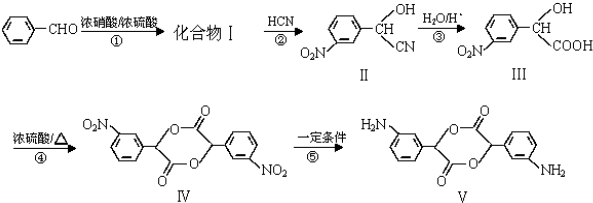
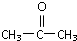 )代替化合物 I发生反应②和反应③可以得到化合物Ⅵ(生产有机玻璃的中间体),则化合物Ⅵ的结构简式为
)代替化合物 I发生反应②和反应③可以得到化合物Ⅵ(生产有机玻璃的中间体),则化合物Ⅵ的结构简式为
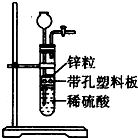 某一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液不足而又无其他酸液可加入.为达到实验目的,则可以从长颈漏斗中加入下列试剂中的①NaN03溶液②酒精③四氯化碳 ④苯⑤Na2C03溶液⑥KCl溶液.( )
某一兴趣小组准备在实验室中制H2,装置如图所示.可是在实验室中发现酸液不足而又无其他酸液可加入.为达到实验目的,则可以从长颈漏斗中加入下列试剂中的①NaN03溶液②酒精③四氯化碳 ④苯⑤Na2C03溶液⑥KCl溶液.( )