��Ŀ����
(8��) ����þ��ҽ���Ͼ��������εȹ�Ч������þ����Ҫ�ɷ���MgCO3��Ϊ��Ҫԭ���Ʊ�����þ�ķ������£�
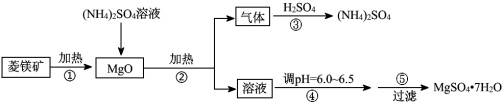
��1��������з�����Ӧ�����ӷ���ʽΪ ��
��2��������е���pH=6.0~6.5��Ŀ���� ��
��3������ݵIJ���Ϊ
��4����֪���ָʾ�����������ɫ��pH��Χ�����ʾ��
pH | < 8.0 | 8.0 ~ 9.6 | > 9.6 |
��ɫ | ��ɫ | ��ɫ | ��ɫ |
25��ʱ����Mg(OH)2�ı�����Һ�еμ�2�ΰ������ָʾ������Һ�����ֵ���ɫΪ [25��ʱ��Ksp[Mg(OH)2] =5.6��10-12]��
��1�� 2NH4+ + MgO��Mg2+ + 2NH3��+ H2O (2��)
��2������Mg2+ˮ�⣬�Ա�õ���������IJ�Ʒ ��2�֣�
��3������Ũ������ȴ�ᾧ��2�֣� ��4����ɫ��2�֣���
��������
�����������1���������ǿ�������Σ�ˮ��ʹ��Һ�����ԣ����Բ�����з�����Ӧ�����ӷ���ʽΪ2NH4+ + MgO��Mg2++ 2NH3��+ H2O����2��������е���pH=6.0~6.5��Ŀ��������Mg2+ˮ�⣬�Ա�õ���������IJ�Ʒ����3������ݵIJ���Ϊ����Ũ������ȴ�ᾧ����4��������25��ʱ��Mg(OH)2�ı�����Һ��c(Mg2+)=x��c(OH-)=2x��x��(2x)2=5.6��10-12;���x=1.13��10-4;����c(OH-)=2.26��10-4; ������Һ��pH=9.7, ��Mg(OH)2�ı�����Һ�еμ�2�ΰ������ָʾ������Һ�����ֵ���ɫΪ��ɫ��
���㣺����������ȡԭ������Ҫ�����ε�ˮ�⡢�����ܽ�ƽ�⡢�����ķ��������������Ŀ�ĵ�֪ʶ��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�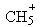 �����ĵ�����Ϊ11NA
�����ĵ�����Ϊ11NA
 2Z(g)���й�����ͼ���˵����ȷ����
2Z(g)���й�����ͼ���˵����ȷ����