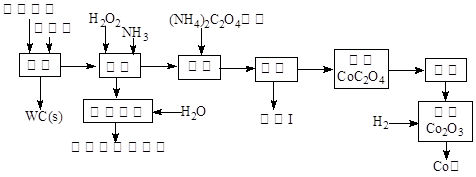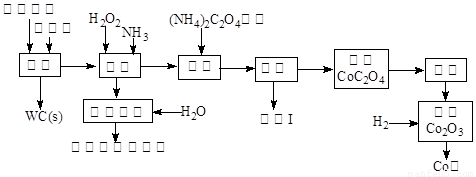题目内容
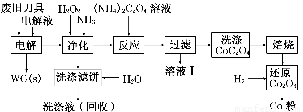
废旧硬质合金刀具中含碳化钨(WC)、金属钴(Co)及少量杂质铁,利用电解法可回收WC和Co.工艺流程简图如下:
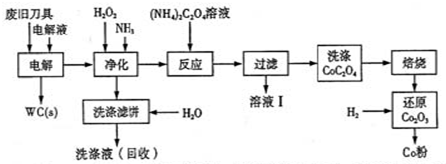
(1)电解时废旧刀具做阳极,不锈钢做阴极,HCl溶液为电解液.阴极主要的电极反应为 .
(2)净化步骤所得滤饼的主要成分是 .回收的洗涤液代替水配制电解液,目的是回收利用其中的 .
(3)溶液I的主要成分是 .洗涤CoC2O4不充分对最终产品纯度并无明显影响,但焙烧时会造成环境污染,原因是 .
(4)将Co2O3还原成Co粉的化学方程式为 .

(1)电解时废旧刀具做阳极,不锈钢做阴极,HCl溶液为电解液.阴极主要的电极反应为
(2)净化步骤所得滤饼的主要成分是
(3)溶液I的主要成分是
(4)将Co2O3还原成Co粉的化学方程式为
分析:(1)电解时阴极得到电子,由于HCl是电解质溶液,所以阴极是氢离子放电生成氢气;
(2)电解时阳极是铁失去电子,生成亚铁离子.然后加入双氧水将亚铁离子氧化生成铁离子,在加入氨水则生成氢氧化铁沉淀,即净化步骤所得滤饼的主要成分是Fe(OH)3;
回收的洗涤液中含有Co2+,因此目的是回收利用其中的Co2+;
(3)由于电解质溶液是盐酸,在反应过程中加入了氨水和草酸铵,所以过滤后溶液I的主要成分是NH4Cl;
洗涤CoC2O4不充分,会附着氯化铵,在煅烧是氯化铵分解生成氨气和氯化氢,从而造成环境污染.
(4)氢气还原Co2O3生成CO粉的同时,还有水生成.
(2)电解时阳极是铁失去电子,生成亚铁离子.然后加入双氧水将亚铁离子氧化生成铁离子,在加入氨水则生成氢氧化铁沉淀,即净化步骤所得滤饼的主要成分是Fe(OH)3;
回收的洗涤液中含有Co2+,因此目的是回收利用其中的Co2+;
(3)由于电解质溶液是盐酸,在反应过程中加入了氨水和草酸铵,所以过滤后溶液I的主要成分是NH4Cl;
洗涤CoC2O4不充分,会附着氯化铵,在煅烧是氯化铵分解生成氨气和氯化氢,从而造成环境污染.
(4)氢气还原Co2O3生成CO粉的同时,还有水生成.
解答:解:(1)电解时阴极得到电子,由于HCl是电解质溶液,所以阴极是氢离子放电生成氢气,电极反应式是2H++2e-=H2↑,
故答案为:2H++2e-=H2↑;
(2)电解时阳极是铁失去电子,生成亚铁离子.然后加入双氧水将亚铁离子氧化生成铁离子,在加入氨水则生成氢氧化铁沉淀,即净化步骤所得滤饼的主要成分是
Fe(OH)3;回收的洗涤液中含有Co2+,因此目的是回收利用其中的Co2+,
故答案为:Fe(OH)3;Co2+;
(3)由于电解质溶液是盐酸,在反应过程中加入了氨水和草酸铵,所以过滤后溶液I的主要成分是NH4Cl;
洗涤CoC2O4不充分,会附着氯化铵,在煅烧是氯化铵分解生成氨气和氯化氢,从而造成环境污染.
故答案为:NH4Cl;焙烧时NH4Cl分解放出 NH3 和HCl气体;
(4)氢气还原Co2O3生成CO粉的同时,还有水生成,反应的化学方程式是3H2+Co2O3
2Co+3H2O,
故答案为:3H2+Co2O3
2Co+3H2O.
故答案为:2H++2e-=H2↑;
(2)电解时阳极是铁失去电子,生成亚铁离子.然后加入双氧水将亚铁离子氧化生成铁离子,在加入氨水则生成氢氧化铁沉淀,即净化步骤所得滤饼的主要成分是
Fe(OH)3;回收的洗涤液中含有Co2+,因此目的是回收利用其中的Co2+,
故答案为:Fe(OH)3;Co2+;
(3)由于电解质溶液是盐酸,在反应过程中加入了氨水和草酸铵,所以过滤后溶液I的主要成分是NH4Cl;
洗涤CoC2O4不充分,会附着氯化铵,在煅烧是氯化铵分解生成氨气和氯化氢,从而造成环境污染.
故答案为:NH4Cl;焙烧时NH4Cl分解放出 NH3 和HCl气体;
(4)氢气还原Co2O3生成CO粉的同时,还有水生成,反应的化学方程式是3H2+Co2O3
| ||
故答案为:3H2+Co2O3
| ||
点评:本题以电解法回收WC和Co工艺流程为载体,考查电解原理、对工艺流程的理解、常用化学用语等,难度中等,理解工艺流程是解题的关键,需要学生具有扎实的基础与综合运用知识分析、解决问题的能力.

练习册系列答案
相关题目