题目内容
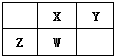 短周期元素X、Y、Z、W在元素周期表中的位置如图所示,其中X形成化合物种类最多,下列说法正确的是( )
短周期元素X、Y、Z、W在元素周期表中的位置如图所示,其中X形成化合物种类最多,下列说法正确的是( )| A、W位于第三周期IV族 |
| B、Y的气态氢化物的水溶液中只存在两个平衡状态 |
C、X的最高价氧化物的电子式是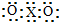 |
| D、常温下,将Z单质投入到Y的最高价氧化物对应的水化物的浓溶液中,无明显现象 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:短周期元素X、Y、Z、W,根据元素在周期表中的位置知,X和Y属于第二周期元素、Z和W属于第三周期元素,其中X形成化合物种类最多,则X是C元素,那么Y是N元素、Z是Al元素、W是Si元素,
A.W位于第三周期第IVA族;
B.Y的气态氢化物为NH3,氨水中存在3个平衡状态;
C.X的最高价氧化物为二氧化碳,二氧化碳分子中每个O原子和C原子形成两个共用电子对;
D.常温下,Al和浓硝酸发生钝化现象.
A.W位于第三周期第IVA族;
B.Y的气态氢化物为NH3,氨水中存在3个平衡状态;
C.X的最高价氧化物为二氧化碳,二氧化碳分子中每个O原子和C原子形成两个共用电子对;
D.常温下,Al和浓硝酸发生钝化现象.
解答:
解:短周期元素X、Y、Z、W,根据元素在周期表中的位置知,X和Y属于第二周期元素、Z和W属于第三周期元素,其中X形成化合物种类最多,则X是C元素,那么Y是N元素、Z是Al元素、W是Si元素,
A.W是Si元素,位于第三周期第IVA族,故A错误;
B.Y的气态氢化物为NH3,存在NH3+H2O?NH3.H2O?NH4++OH-、H2O?H++OH-,所以氨水中存在3个平衡状态,故B错误;
C.X的最高价氧化物为二氧化碳,二氧化碳分子中每个O原子和C原子形成两个共用电子对,其电子式为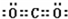 ,故C错误;
,故C错误;
D.常温下,Al和浓硝酸发生氧化还原反应而生成一层致密的氧化物薄膜而阻止进一步被氧化,该现象为钝化现象,所以将Z单质投入到Y的最高价氧化物对应的水化物的浓溶液中,无明显现象,故D正确;
故选D.
A.W是Si元素,位于第三周期第IVA族,故A错误;
B.Y的气态氢化物为NH3,存在NH3+H2O?NH3.H2O?NH4++OH-、H2O?H++OH-,所以氨水中存在3个平衡状态,故B错误;
C.X的最高价氧化物为二氧化碳,二氧化碳分子中每个O原子和C原子形成两个共用电子对,其电子式为
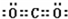 ,故C错误;
,故C错误;D.常温下,Al和浓硝酸发生氧化还原反应而生成一层致密的氧化物薄膜而阻止进一步被氧化,该现象为钝化现象,所以将Z单质投入到Y的最高价氧化物对应的水化物的浓溶液中,无明显现象,故D正确;
故选D.
点评:本题考查了元素周期表和元素周期律的综合应用,注意确定元素在周期表中的位置时要注明周期数、族序数,注意B中还存在水的电离平衡,为易错点.

练习册系列答案
相关题目
只用一种试剂就能进行鉴别的是( )
| A、FeO、Fe(粉)、CuO、C |
| B、(NH4)2SO4、NH4Cl、NaNO3、NaCl |
| C、乙醛、乙酸、甲酸、乙醇 |
| D、苯、四氯化碳、溴乙烷、己烯 |
长周期元素周期表共有18个竖行,从左到右排为1~18列,即碱金属是第一列,稀有气体是第18列.按这种规定,下面说法正确的是( )
| A、第13列元素中没有非金属 |
| B、第15列元素的原子最外层的排布是ns2np3 |
| C、最外层电子数为ns2的元素在第2列 |
| D、10、11列为ds区的元素 |
下列说法正确的是( )
| A、分子式相同而结构不同的有机物一定互为同分异构体 |
| B、具有同一通式、分子组成上相差若干个CH2原子团的物质一定属于同系物 |
| C、组成元素相同、结构不同的有机物都互为同分异构体 |
| D、只要相对分子质量相同就一定属于同分异构体 |
粗盐提纯实验用到的试剂中,不是为了除去原溶液中杂质离子的是( )
| A、盐酸 | B、烧碱溶液 |
| C、纯碱溶液 | D、氯化钡溶液 |
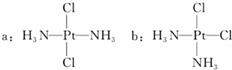 科学家发现铂的两种化合物a和b(见图),实验测得a和b具有不同的性质,且a具有抗癌作用,而b没有.下列关于a、b的叙述错误的是( )
科学家发现铂的两种化合物a和b(见图),实验测得a和b具有不同的性质,且a具有抗癌作用,而b没有.下列关于a、b的叙述错误的是( )| A、a和b互为同分异构体 |
| B、a和b互为“镜”和“像”的关系 |
| C、a和b的空间构型是平面四边形 |
| D、a和b分别是非极性分子和极性分子 |
25℃时加水稀释10mL pH=11的氨水,下列判断正确的是( )
| A、原氨水的浓度=10-3mol/L | ||||
B、溶液中
| ||||
| C、氨水的电离程度增大,溶液中所有离子的浓度均减小 | ||||
| D、再加入10mL pH=3的盐酸充分反应后混合液的pH值肯定大于7 |
 用如图所示装置进行实验,将少量液体甲逐滴加入到固体乙中,试管中试剂为丙,则下表中现象与结论均正确的是( )
用如图所示装置进行实验,将少量液体甲逐滴加入到固体乙中,试管中试剂为丙,则下表中现象与结论均正确的是( )