题目内容
已知
(1)H2( g )+
O2 ( g )=H2O ( g )△H1=a kJ/mol
(2)2H2( g )+O2 ( g )=2H2O ( g )△H2=b kJ/mol
(3)H2( g )+
O2 ( g )=H2O ( l )△H3=c kJ/mol
(4)2H2( g )+O2 ( g )=2H2O ( l )△H4=d kJ/mol
则a、b、c、d的关系正确的是( )
(1)H2( g )+
| 1 |
| 2 |
(2)2H2( g )+O2 ( g )=2H2O ( g )△H2=b kJ/mol
(3)H2( g )+
| 1 |
| 2 |
(4)2H2( g )+O2 ( g )=2H2O ( l )△H4=d kJ/mol
则a、b、c、d的关系正确的是( )
| A、c<a<0 |
| B、b>d>0 |
| C、2a=b<0 |
| D、2c=d>0 |
考点:反应热的大小比较
专题:化学反应中的能量变化
分析:物质的燃烧是放热的,焓变是负值,氢气燃烧生成的水从液态变为气态会吸收热,化学方程式系数加倍,焓变数值也要加倍,符号不变,据此回答.
解答:
解:氢气的燃烧是放热的,焓变是负值,所以a、b、c、d都是小于零的,方程式的系数(2)是(1)的2倍,(4)是(3)的2倍,所以2a=b<0,2c=d<0,故B、D错误,C正确;氢气燃烧生成的水从液态变为气态会吸收热,所以c<a<0,故A正确.
故选AC.
故选AC.
点评:本题是一道关于反应热的大小比较的考查题,注意物质的燃烧是放热的,且焓变是带符号的,难度不大.

练习册系列答案
相关题目
下列分子的中心原子杂化轨道的类型相同的是( )
| A、BeCl2和BF3 |
| B、H2O和NH3 |
| C、CO2和SO2 |
| D、HCHO和PCl3 |
下列图象分别表示有关反应的反应过程与能量变化的关系,其中错误的是( )


| A、石墨转变为金刚石是吸热反应 |
| B、白磷比红磷稳定 |
| C、S(g)+O2(g)=SO2 (g)△H1;S (s)+O2(g)=SO2(g)△H2,则△H1>△H2 |
| D、CO(g)+H2O(g)=CO2(g)+H2(g)△H>0 |
现有等浓度的下列溶液:①醋酸,②硫酸氢钠,③醋酸钠,④碳酸,⑤碳酸钠,⑥硫酸钠.按溶液pH由小到大排列正确的是
( )
( )
| A、④①②⑤⑥③ |
| B、⑥①②④③⑤ |
| C、②①④⑥③⑤ |
| D、①④②③⑥⑤ |
下列反应属于加成反应的是( )
| A、2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ |
B、 |
C、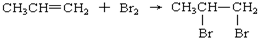 |
D、 |
下列物质呈酸性且与Na反应生成H2的是( )
| A、H2O |
| B、CH3CH2OH |
C、 |
| D、CH3COOH |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,22.4LCC14中含有的分子数目为NA |
| B、25℃时,1 L pH=1的醋酸溶液中含有醋酸分子数大于0.1 NA |
| C、含0.1 mol FeCl3的饱和溶液中Fe3+数目为0.1 NA |
| D、常温常压下,0.1mo1C12溶于足量NaOH溶液中,转移的电子数目为0.2NA |
在给定的四种溶液中,各离子能在溶液中大量共存的有( )
| A、无色溶液:Al3+、K+、Cl-、[Al(OH)4]- |
| B、c(OH-)=10-13mol/L的溶液:Cu2+、Na+、Mg2+、NO3- |
| C、由水电离出来的c(H+)=10-13mol/L的溶液:Fe2+、NH4+、Cl-、NO3- |
| D、滴加石蕊试液显红色的溶液:K+、HCO3-、Br-、Ba2+ |
实验中剩余的药品应( )
| A、放回原瓶 |
| B、拿出实验室 |
| C、放入垃圾筒 |
| D、放入指定容器 |