题目内容
1.设NA为阿伏加德罗常数的值,下列说法正确的是( )| A. | 28g N2所含的原子数目为NA | |
| B. | 标准状况下,18 g H2O所占的体积约为22.4 L | |
| C. | 0.5 mol H2SO4含有的原子数目为3.5NA | |
| D. | 在常温常压下,11.2 L N2含有的原子数为NA |
分析 A、氮气由氮原子构成;
B、标况下水为液态;
C、硫酸为7原子分子;
D、常温常压下,气体摩尔体积大于22.4L/mol.
解答 解:A、氮气由氮原子构成,故28g氮气中含有的氮原子的物质的量为n=$\frac{28g}{14g/mol}$=2mol,故个数为2NA个,故A错误;
B、标况下水为液态,故18g水即1mol水的体积小于22.4L,故B错误;
C、硫酸为7原子分子,故0.5mol硫酸中含3.5NA个原子,故C正确;
D、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L氮气的物质的量小于0.5mol,则含有的原子个数小于NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
12.下列实验操作与实验目的相对应的是( )
| 实验操作 | 实验目的 | |
| A | 制乙炔时用饱和食盐水代替水 | 加快化学反应速率 |
| B | C2H4与SO2混合气体通过盛有溴水的洗气瓶 | 除去C2H4中的SO2 |
| C | 淀粉溶液水解后冷却至室温,加碘水观察现象 | 检验淀粉是否完全水解 |
| D | 将溴乙烷与氢氧化钠水溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 | 检验溴乙烷中的溴原子 |
| A. | A | B. | B | C. | C | D. | D |
9.下列有关化学用语的表示正确的是( )
| A. | 氯分子的电子式: | |
| B. | 氯离子(Cl-)的结构示意图: | |
| C. | 质子数为17、中子数为20的氯原子:${\;}_{17}^{20}$Cl | |
| D. | 二氧化碳分子的结构式:O-C-O |
6.下列物质不能为动物体提供能量的是( )
| A. | 脂肪 | B. | 蛋白质 | C. | 微量元素 | D. | 糖类 |
13.甲、乙两容器中都在进行A?B+C的反应,甲中每分钟减少4mol A,乙中每分钟减少2mol A,则甲、乙两容器中的反应速率的比较是( )
| A. | 甲快 | B. | 乙快 | C. | 相等 | D. | 无法确定 |
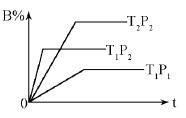
 pC(g) △H=Q kJ·mol-1,在密闭容器中进行,下图表示在不同时间t、温度T、压强P与反应物B的百分含量的关系曲线,下列判断正确的是
pC(g) △H=Q kJ·mol-1,在密闭容器中进行,下图表示在不同时间t、温度T、压强P与反应物B的百分含量的关系曲线,下列判断正确的是