题目内容
(1)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ,则该反应的热化学方程式应为 .
(2)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式 .若1g水蒸气转化成液态水放热2.444kJ,则反应2H2(g)+O2(g)═2H2O(l)的△H= ,氢气的燃烧热为 .
(3)已知0.5mol甲烷与0.5mol水蒸气在t℃.p kPa时,完全反应生成一氧化碳和氢气,吸收了a kJ热量,该反应的热化学方程式是: .
(2)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式
(3)已知0.5mol甲烷与0.5mol水蒸气在t℃.p kPa时,完全反应生成一氧化碳和氢气,吸收了a kJ热量,该反应的热化学方程式是:
考点:热化学方程式,反应热和焓变
专题:化学反应中的能量变化
分析:(1)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ,则32g甲醇即1mol甲醇完全燃烧生成二氧化碳和液态水放出的热量=
×32g=725.8kJ;
(2)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,生成2mol水蒸气放出热量为483.6kJ,该反应热化学反应方程式为2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol,若1g水蒸气转化成液态水放热2.444kJ,则1mol水蒸气转化为液态水放出热量=
=43.992kJ/mol,根据盖斯定律计算其焓变;
(3)0.5mol甲烷与0.5mol水蒸气在t℃.p kPa时,完全反应生成一氧化碳和氢气,吸收了a kJ热量,则1mol甲烷和1mol水蒸气在t℃.p kPa时,完全反应生成一氧化碳和氢气,吸收了2a kJ热量,据此书写其热化学反应方程式.
| 22.68kJ |
| 1g |
(2)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,生成2mol水蒸气放出热量为483.6kJ,该反应热化学反应方程式为2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol,若1g水蒸气转化成液态水放热2.444kJ,则1mol水蒸气转化为液态水放出热量=
| 2.444kJ | ||
|
(3)0.5mol甲烷与0.5mol水蒸气在t℃.p kPa时,完全反应生成一氧化碳和氢气,吸收了a kJ热量,则1mol甲烷和1mol水蒸气在t℃.p kPa时,完全反应生成一氧化碳和氢气,吸收了2a kJ热量,据此书写其热化学反应方程式.
解答:
解:(1)在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ,则32g甲醇即1mol甲醇完全燃烧生成二氧化碳和液态水放出的热量=
×32g=725.8kJ,其热化学反应方程式为CH3OH(l)+
O2(g)=CO2(g)+2H2O(l)△H=-725.8KJ/mol,
故答案为:CH3OH(l)+
O2(g)=CO2(g)+2H2O(l)△H=-725.8KJ/mol;
(2)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,生成2mol水蒸气放出热量为483.6kJ,该反应热化学反应方程式为2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol,若1g水蒸气转化成液态水放热2.444kJ,则1mol水蒸气转化为液态水放出热量=
=43.992kJ/mol,根据盖斯定律知其焓变=
-483.6kJ/mol+(-43.992kJ/mol)×2=-571.58kJ/mol,则氢气的燃烧热=
=285.8kJ/mol,
故答案为:2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol;-571.58kJ/mol;285.8kJ/mol;
(3)0.5mol甲烷与0.5mol水蒸气在t℃.p kPa时,完全反应生成一氧化碳和氢气,吸收了a kJ热量,则1mol甲烷和1mol水蒸气在t℃.p kPa时,完全反应生成一氧化碳和氢气,吸收了2a kJ热量,所以其热化学反应方程式为CH4(g)+H2O(g)=CO(g)+3H2(g)△H=-2akJ/mol,
故答案为:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=-2akJ/mol.
| 22.68kJ |
| 1g |
| 3 |
| 2 |
故答案为:CH3OH(l)+
| 3 |
| 2 |
(2)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,生成2mol水蒸气放出热量为483.6kJ,该反应热化学反应方程式为2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol,若1g水蒸气转化成液态水放热2.444kJ,则1mol水蒸气转化为液态水放出热量=
| 2.444kJ | ||
|
-483.6kJ/mol+(-43.992kJ/mol)×2=-571.58kJ/mol,则氢气的燃烧热=
| 571.58kJ/mol |
| 2 |
故答案为:2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol;-571.58kJ/mol;285.8kJ/mol;
(3)0.5mol甲烷与0.5mol水蒸气在t℃.p kPa时,完全反应生成一氧化碳和氢气,吸收了a kJ热量,则1mol甲烷和1mol水蒸气在t℃.p kPa时,完全反应生成一氧化碳和氢气,吸收了2a kJ热量,所以其热化学反应方程式为CH4(g)+H2O(g)=CO(g)+3H2(g)△H=-2akJ/mol,
故答案为:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=-2akJ/mol.
点评:本题考查热化学反应方程式的书写,注意焓变与反应物的物质的量、物质状态都有关,侧重考查学生计算能力,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
下列过程属于人工固氮的是( )
| A、分离液态空气制氮气 |
| B、闪电时N2 转化为NO |
| C、合成氨 |
| D、豆科作物根瘤菌将N2 转化为NH3 |
下列有关工业生产的叙述正确的是( )
| A、合成氨工业中,将NH3及时液化分离有利于加快反应速率 |
| B、氯碱工业中,使用离子交换膜可防止Cl2和NaOH溶液反应 |
| C、硫酸工业中,接触室内安装热交换器,是为了利用沸腾炉中排出的SO2的热量 |
| D、硫酸工业中,SO2的催化氧化不采用高压,是因为压强对SO2转化率无影响 |
碳酸铜和碱式碳酸铜均可溶于盐酸,转化为氯化铜.在高温下这两种化合物均能分解成氧化铜.溶解28.4g上述混合物,消耗1mol/L盐酸500mL.灼烧等质量的上述混合物,得到氧化铜的质量是( )
| A、35g |
| B、30 g |
| C、20 g |
| D、15 g |
下列实验操作或做法正确的是( )
| A、用托盘天平称量5.85 g氯化钠固体 |
| B、从试剂瓶中取Na2CO3溶液,发现取量过多,为了不浪费,把过量的试剂倒入原试剂瓶中 |
| C、用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 |
| D、用蒸发的方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干 |
下列实验操作中错误的是( )
| A、进行蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| B、进行萃取操作时,应选择有机萃取剂 |
| C、进行蒸发操作时,至当出现大量固体时,应停止加热用余热蒸干 |
| D、进行分液操作时,分液漏斗中下层液体从下口放出后,换一洁净烧杯继续接取上层液体 |
 可逆反应mX(g)+nY(g)?pZ(g),在不同的温度(T1、T2)和不同的压强(P1、P2)下,产物Z的物质的量(n)与时间(t)的关系如图所示,则下列判断正确的是( )
可逆反应mX(g)+nY(g)?pZ(g),在不同的温度(T1、T2)和不同的压强(P1、P2)下,产物Z的物质的量(n)与时间(t)的关系如图所示,则下列判断正确的是( )| A、m+n<p |
| B、m+n>p |
| C、增大压强平衡向正反应方向移动 |
| D、升高温度平衡向正反应方向移动 |
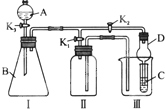 某兴趣小组的同学共同设置了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质.请回答下列问题:
某兴趣小组的同学共同设置了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质.请回答下列问题: