题目内容
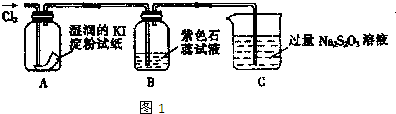
有一瓶澄清的溶液,其中可能含有NH4+、K+、Ba2+、Al3+、Fe3+、I-、NO3-、CO32-、SO42-、AlO2-.取该溶液进行以下实验:
①用pH试纸检验,溶液呈强酸性.
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色.
③另取溶液适量,逐滴加入NaOH溶液:
a.溶液从酸性变为中性;b.溶液逐渐产生沉淀;c.沉淀完全溶解;d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝.
④取适量③得到的碱性溶液加入Na2CO3溶液,有白色沉淀生成.
根据上述实验现象,回答下列问题.
(1)由①可以排除 离子的存在.
(2)由②可以证明 离子的存在,同时排除 离子存在.理由是 .
(3)由③可证明 离子存在.
(4)由④可以排除 离子存在,同时证明 离子的存在.
①用pH试纸检验,溶液呈强酸性.
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色.
③另取溶液适量,逐滴加入NaOH溶液:
a.溶液从酸性变为中性;b.溶液逐渐产生沉淀;c.沉淀完全溶解;d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝.
④取适量③得到的碱性溶液加入Na2CO3溶液,有白色沉淀生成.
根据上述实验现象,回答下列问题.
(1)由①可以排除
(2)由②可以证明
(3)由③可证明
(4)由④可以排除
考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题,离子反应专题
分析:①用pH试纸检测,溶液呈强酸性,说明溶液中存在H+,根据离子共存可知,溶液中一定不存在CO32-,AlO2-;
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色,说明溶液中一定含有I-,结合离子共存可知,一定不含有Fe3+、NO3-;
③另取溶液适量,逐滴加入NaOH溶液;
a.溶液从酸性变为中性,氢氧根离子与氢离子发生中和反应;
b.溶液逐渐产生沉淀,分析阳离子中只有铝离子沉淀;
c.沉淀完全溶解,证明生成的沉淀是氢氧化铝,原溶液中一定含有Al3+;
d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝,证明生成的气体是氨气,原溶液中一定含有NH4+;
④取适量③得到的碱性溶液,铝离子反应生成偏铝酸根离子,加入Na2CO3溶液,有白色沉淀生成,只有Ba2+生成碳酸钡沉淀,说明原溶液中一定含有Ba2+,一定不含SO42-;
分解以上分析进行解答.
②取溶液适量,加入少量CCl4和数滴新制氯水,振荡,CCl4层呈紫红色,说明溶液中一定含有I-,结合离子共存可知,一定不含有Fe3+、NO3-;
③另取溶液适量,逐滴加入NaOH溶液;
a.溶液从酸性变为中性,氢氧根离子与氢离子发生中和反应;
b.溶液逐渐产生沉淀,分析阳离子中只有铝离子沉淀;
c.沉淀完全溶解,证明生成的沉淀是氢氧化铝,原溶液中一定含有Al3+;
d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝,证明生成的气体是氨气,原溶液中一定含有NH4+;
④取适量③得到的碱性溶液,铝离子反应生成偏铝酸根离子,加入Na2CO3溶液,有白色沉淀生成,只有Ba2+生成碳酸钡沉淀,说明原溶液中一定含有Ba2+,一定不含SO42-;
分解以上分析进行解答.
解答:
解:(1)①用pH试纸检验,溶液呈强酸性,溶液中存在大量H+,由于CO32-,AlO2-都是弱酸阴离子,二者都能够与氢离子反应,所以CO32-,AlO2- 不能大量存在,
故答案为:CO32-、AlO2-;
(2)②取溶液适量,加入少量CCl4和数滴新制的氯水振荡,四氯化碳层呈紫色,说明溶液中含有I-,由于 Fe3+、NO3-(在酸溶液中)能氧化I-为I2,所以溶液中不存在Fe3+、NO3-,
故答案为:I-;Fe3+、NO3-;CCl4层出现碘单质的颜色证明含I-,Fe3+、NO3-在该环境中与I-不能共存;
(3)③依据题意生成的沉淀又溶解,说明溶液中存在Al3+;
依据加热溶液生成的气体能使湿润的红色石蕊试纸变蓝证明气体是氨气,说明原溶液中含有NH4+,
故答案为:Al3+、NH4+;
(4)④取适量③得到的碱性溶液,加入碳酸钠溶液有白色沉淀生成,说明溶液中一定存在Ba2+,根据离子共存可知,一定不存在SO42-,
故答案为:SO42-;Ba2+.
故答案为:CO32-、AlO2-;
(2)②取溶液适量,加入少量CCl4和数滴新制的氯水振荡,四氯化碳层呈紫色,说明溶液中含有I-,由于 Fe3+、NO3-(在酸溶液中)能氧化I-为I2,所以溶液中不存在Fe3+、NO3-,
故答案为:I-;Fe3+、NO3-;CCl4层出现碘单质的颜色证明含I-,Fe3+、NO3-在该环境中与I-不能共存;
(3)③依据题意生成的沉淀又溶解,说明溶液中存在Al3+;
依据加热溶液生成的气体能使湿润的红色石蕊试纸变蓝证明气体是氨气,说明原溶液中含有NH4+,
故答案为:Al3+、NH4+;
(4)④取适量③得到的碱性溶液,加入碳酸钠溶液有白色沉淀生成,说明溶液中一定存在Ba2+,根据离子共存可知,一定不存在SO42-,
故答案为:SO42-;Ba2+.
点评:本题考查常见离子的检验方法,题目难度中等,注意掌握常见离子的性质及正确的检验方法,要求学生能够根据离子反应的现象判断原溶液中存在的离子名称,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
在A+B(s)?C反应中,若增大压强或降低温度,B的转化率均增大,则反应体系应是( )
| A、A是固体,C是气体,正反应吸热 |
| B、A是气体,C是固体或液体,正反应放热 |
| C、A是气体,C是气体,正反应放热 |
| D、A是气体,C是气体,正反应吸热 |
科学家因发现导电塑料荣获2000年诺贝尔化学奖.导电塑料的结构可表示为[CH=CH]n,则其单体为( )
| A、乙烯 | B、乙炔 |
| C、乙烷 | D、1,3-丁二烯 |
下列变化,需要加入适当的氧化剂才能完成的是( )
| A、CuO→Cu |
| B、Fe→FeCl2 |
| C、H2O2→O2 |
| D、NO2→HNO3 |
下列化学用语表达正确的是( )
| A、N2的结构式::N≡N: |
B、NaCl的电子式: |
| C、Cr的价层电子排布图:3d54s1 |
D、F-的结构示意图: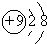 |
已知下列热化学方程式:
①C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
②CO(g)+
O2(g)═CO2(g)△H=-283.0kJ/mol
③2Fe(s)+3CO(g)═Fe2O3(s)+3C(s)△H=-489.0kJ/mol
则4Fe(s)+3O2(g)═2Fe2O3(s)的反应热△H为( )
①C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
②CO(g)+
| 1 |
| 2 |
③2Fe(s)+3CO(g)═Fe2O3(s)+3C(s)△H=-489.0kJ/mol
则4Fe(s)+3O2(g)═2Fe2O3(s)的反应热△H为( )
| A、-1641.0kJ/mol |
| B、+3081kJ/mol |
| C、+663.5kJ/mol |
| D、-2507.0kJ/mol |