题目内容
由CO2、H2和CO组成的混合气在同温同压下与氮气的密度相同.则该混合气体中CO2、H2和CO的体积比不可能为( )
| A、39:24:13 |
| B、22:7:14 |
| C、13:8:29 |
| D、26:16:57 |
考点:有关混合物反应的计算
专题:计算题
分析:根据CO2、H2和CO碳组成的混合气体在同温、同压下与氮气的密度相同,可知混合气体的平均相对分子质量等于氮气的相对分子质量,即为28,而CO的相对分子质量也为28,则二氧化碳与氢气的平均相对分子质量必须为28,据此进行解答.
解答:
解:CO2、H2和CO组成的混合气体在同温、同压下与N2的密度相同,则混合气体的平均相对分子质量等于氮气的相对分子质量,即为28,
由于CO的相对分子质量为28,则CO2和H2的平均相对分子质量为28即可,CO的体积不受限制,
利用十字相乘法得二氧化碳和氢气的体积之比:
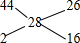
则CO2和H2的体积之比为26:16=13:8,CO的体积为任意体积,所以ACD正确、B错误,
故选B.
由于CO的相对分子质量为28,则CO2和H2的平均相对分子质量为28即可,CO的体积不受限制,
利用十字相乘法得二氧化碳和氢气的体积之比:

则CO2和H2的体积之比为26:16=13:8,CO的体积为任意体积,所以ACD正确、B错误,
故选B.
点评:本题考查混合气体的计算,难度不大,明确相同条件下气体的密度之比等于相对分子质量之比计算即可,试题侧重于学生的分析能力和计算能力的考查,注意把握十字交叉法的运用.

练习册系列答案
相关题目
 如图是向MgCl2、AlCl3混合溶液中,先后加入试剂A、B时所得沉淀物质的量y(mol) 与试剂体积V(mL)间的关系图.开始滴加6mL试剂A后继续滴加A若干,之后改滴试剂B.以下结论正确的是( )
如图是向MgCl2、AlCl3混合溶液中,先后加入试剂A、B时所得沉淀物质的量y(mol) 与试剂体积V(mL)间的关系图.开始滴加6mL试剂A后继续滴加A若干,之后改滴试剂B.以下结论正确的是( )| A、A可能是NaOH,B可能是盐酸,且2cA=cB |
| B、原混合液中,c(Al3+):c(Mg2+):c(Cl-)=1:2:7 |
| C、A可能是Ba(OH)2,B可能是硫酸,且cA=2cB |
| D、若A和B均为一元强酸或一元强碱,则滴加7mL试剂A后改滴试剂B |
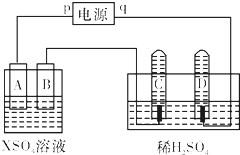 如图,p、q为直流电源的两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D极上均产生气泡.试回答:
如图,p、q为直流电源的两极,A由+2价金属单质X制成,B、C、D为铂电极,接通电源,金属X沉积于B极,同时C、D极上均产生气泡.试回答: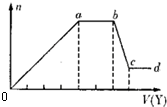 ①若Y是盐酸,则溶液中含有的金属阳离子是
①若Y是盐酸,则溶液中含有的金属阳离子是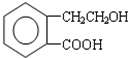 ,它可通过不同化学反应分别制得B、C和D 三种物质.
,它可通过不同化学反应分别制得B、C和D 三种物质.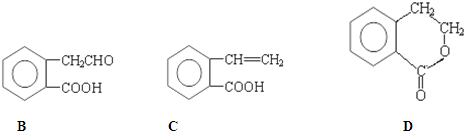
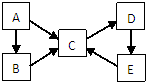 A、B、C、D、E五种物质(或离子)均含有同一种元素,它们之间有如下转化关系:
A、B、C、D、E五种物质(或离子)均含有同一种元素,它们之间有如下转化关系: