题目内容
17.下列各组物质中,能用高锰酸钾酸性溶液鉴别的是( )| A. | 乙烯、乙炔 | B. | 1-己烯、苯 | C. | 苯、正已烷 | D. | 甲苯、2-己烯 |
分析 含碳碳双键、三键的有机物及苯的同系物能被高锰酸钾氧化,烷烃、苯不能被高锰酸钾氧化,以此来解答.
解答 解:A.乙烯、乙炔均使高锰酸钾酸性溶液褪色,不能鉴别,故A不选;
B.1-己烯使高锰酸钾褪色,苯不能,现象不同,可鉴别,故B选;
C.苯、正已烷均与高锰酸钾不反应,不能鉴别,故C不选;
D.甲苯、2-己烯均使高锰酸钾酸性溶液褪色,不能鉴别,故D不选;
故选B.
点评 本题考查有机物的鉴别,为高频考点,把握有机物的性质、性质差异为解答的关键,侧重分析与应用能力的考查,注意有机物性质的应用,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.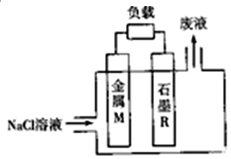 金属染料电池是一类特殊的染料电池,具有成本低、无毒、无污染、比功率高、比能量高(比能量可用单位质量金属提供电子多少来表示)等优点.锌、铁、铝、锂等金属都可用在金属燃料电池中,电池的基本结构如图所示:下列说法正确的是( )
金属染料电池是一类特殊的染料电池,具有成本低、无毒、无污染、比功率高、比能量高(比能量可用单位质量金属提供电子多少来表示)等优点.锌、铁、铝、锂等金属都可用在金属燃料电池中,电池的基本结构如图所示:下列说法正确的是( )
 金属染料电池是一类特殊的染料电池,具有成本低、无毒、无污染、比功率高、比能量高(比能量可用单位质量金属提供电子多少来表示)等优点.锌、铁、铝、锂等金属都可用在金属燃料电池中,电池的基本结构如图所示:下列说法正确的是( )
金属染料电池是一类特殊的染料电池,具有成本低、无毒、无污染、比功率高、比能量高(比能量可用单位质量金属提供电子多少来表示)等优点.锌、铁、铝、锂等金属都可用在金属燃料电池中,电池的基本结构如图所示:下列说法正确的是( )| A. | 电池工作时,电子沿M电极→电解质溶液→R电极流动 | |
| B. | 电池工作时,正极附近溶液的pH增大 | |
| C. | 在锌、铁、铝、锂中,锂的比能量最高 | |
| D. | 若M为锌时,电池反应为 Zn+2H2O═Zn(OH)2+H2↑ |
8.下列说法正确的是( )
| A. | 工业上常用二氧化硫来漂白纸浆、丝毛、草帽以及给食品增白 | |
| B. | 浓硫酸可以用来干燥SO2、CO2 H2等气体 | |
| C. | 硫粉在过量的纯氧中燃烧可以生成SO3 | |
| D. | 稀硝酸在空气中可以通过加热浓缩的方法增大溶液的浓度 |
5.现有X、Y、Z、W四种金属片,①把X、Y用导线连接后同时浸入稀硫酸溶液中,X上有气泡产生,Y溶解;②把Z、W用导线连接后同时浸入稀硫酸溶液中,W发生还原反应;③把X、Z用导线连接后同时浸入稀硫酸溶液中,电子流动方向为X→导线→Z.根据上述情况判断正确的是( )
| A. | 在①中金属片Y发生还原反应 | |
| B. | 在②中金属片W作负极 | |
| C. | 上述四种金属的活动性顺序为W<X<Z<Y | |
| D. | 如果把Y、W用导线相连后同时浸入稀硫酸溶液,则电子流动方向为Y→导线→W |
12.已知镓和铝在周期表中位于同一纵行,氮化镓可把手机信号扩大10倍,让电脑的速度提高1万倍,将CD缩减到1英寸,下列有关氮化镓的说法中正确的是( )
| A. | 氮化镓是由主族元素与副族元素形成的化合物 | |
| B. | 镓元素比铝元素金属性弱 | |
| C. | 氮化镓中氮元素显+3价 | |
| D. | 氮原子最外层比镓原子最外层多2个电子 |
2.下列各组中每种物质都既有离子键又有共价键的一组是( )
| A. | NaOH、H2SO4、(NH4)2SO4 | B. | Ba(OH)2、Na2SO4、Na3PO4 | ||
| C. | Na2CO3、HNO3、MgO | D. | HCl、Al2O3、MgCl2 |
9.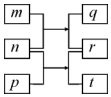 短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,r为一元强酸,t通常是固态单质.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,r为一元强酸,t通常是固态单质.上述物质的转化关系如图所示.下列说法正确的是( )
 短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,r为一元强酸,t通常是固态单质.上述物质的转化关系如图所示.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,r为一元强酸,t通常是固态单质.上述物质的转化关系如图所示.下列说法正确的是( )| A. | 原子半径的大小W>X>Y | B. | 元素的非金属性Z>X>Y | ||
| C. | X的氢化物常温常压下为液态 | D. | Y的最高价氧化物的水化物为弱酸 |
6.下列事实不能作为实验判断依据的是( )
| A. | 钠和镁分别与冷水反应,判断金属活动性强弱:Na>Mg | |
| B. | 铁投入CuSO4溶液中,能置换出铜,钠投入CuSO4溶液中不能置换出铜,判断钠与铁的金属活动性强弱:Cu>Na | |
| C. | 酸性H2CO3<H2SO4,判断硫与碳的非金属性强弱:S>C | |
| D. | F2与Cl2分别与H2反应,判断氟与氯的非金属性强弱:F>Cl |
2.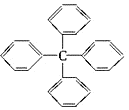 甲烷分子中的四个氢原子都可以被取代.若甲烷分子中的四个氢原子都被苯基取代,则可得到新分子(如图). 对该分子的描述不正确的是( )
甲烷分子中的四个氢原子都可以被取代.若甲烷分子中的四个氢原子都被苯基取代,则可得到新分子(如图). 对该分子的描述不正确的是( )
 甲烷分子中的四个氢原子都可以被取代.若甲烷分子中的四个氢原子都被苯基取代,则可得到新分子(如图). 对该分子的描述不正确的是( )
甲烷分子中的四个氢原子都可以被取代.若甲烷分子中的四个氢原子都被苯基取代,则可得到新分子(如图). 对该分子的描述不正确的是( )| A. | 分子式为C25H20 | B. | 属于芳香烃 | ||
| C. | 该物质的一氯代物有3种 | D. | 所有碳原子可能都在同一平面上 |