题目内容
14.在分子式为CnH2n的烃分子中共用电子对的数目为( )| A. | 3n | B. | 3n+1 | C. | 2n | D. | 2n+1 |
分析 分子式为CnH2n的烃分子要么是单烯烃,要么是环烷烃,但无论结构如何,对共用电子对数无影响.
解答 解:分子式为CnH2n的烃分子要么是单烯烃,要么是环烷烃,但无论是哪种结构,在C原子和H原子间均存在2n对共用电子对,在碳原子间均存在n对共用电子对,故共存在3n对共用电子对,故选A.
点评 本题考查了烃分子中共用电子对的对数,应注意的是有几个H原子即在C和H原子间存在几对共用电子对,然后根据C原子间的成键情况来分析C原子间的共用电子对.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
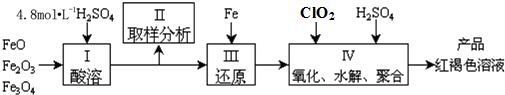
5.铜及其化合物在工农业生产及日常生活中应用非常广泛.某研究小组用粗铜(含杂质铁)制备氯化铜晶体(CuCl2•2H2O )的流程如下.

已知常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
请回答下列问题:
(1)溶液I中加入试剂X可以调节溶液pH,从而除去Fe3+且不引入杂质.
①试剂X可选用下列物质中的ad(填代号).
a.CuO b.NaOH c.Cu d.Cu(OH)2
②调节溶液pH时,理论上可选择pH最大范围是3.2≤pH<4.7.
(2)由溶液Ⅱ制备CuCl2•2H2O的操作依次为:边滴加浓盐酸边加热浓缩、冷却结晶(填操作名称)、过滤、洗涤干燥.
(3)室温下,将NaOH溶液逐滴加入到浓度均为0.1mol/L的MgCl2和CuCl2混合溶液中,先生成的沉淀是Cu(OH)2.(室温时KSP[Mg(OH)2]=1.8×10-11,KSP[Cu(OH)2]=2.2×10-20)
(4)某学习小组用碘量法测定CuCl2•2H2O样品的纯度(杂质不与发生反应).实验如下:
a.准确称取CuCl2•2H2O样品mg于小烧杯中,加入适量蒸馏水和足量的碘化钾,再滴入适量的稀硫酸,充分反应后,将所得混合液配成250mL待测溶液.(已知:2Cu2++4I-═2CuI+I2)
b.移取25.00mL待测溶液于锥形瓶中,加几滴指示剂,用c mol•L-1Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为V mL.(已知:I2+2S2O32-═2I-+S4O62-)
①实验中使用的指示剂名称为淀粉,达到滴定终点时的溶液颜色变化为溶液由蓝色变为无色.
②该样品中CuCl2•2H2O 的质量分数为$\frac{{171cV×{{10}^{-3}}×10}}{m}×100%$(用含m、c、V的代数式表示,不用化简).

已知常温下,Cu2+、Fe3+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
| 金属离子 | Fe3+ | Cu2+ |
| 氢氧化物开始沉淀时的pH | 1.9 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 6.7 |
(1)溶液I中加入试剂X可以调节溶液pH,从而除去Fe3+且不引入杂质.
①试剂X可选用下列物质中的ad(填代号).
a.CuO b.NaOH c.Cu d.Cu(OH)2
②调节溶液pH时,理论上可选择pH最大范围是3.2≤pH<4.7.
(2)由溶液Ⅱ制备CuCl2•2H2O的操作依次为:边滴加浓盐酸边加热浓缩、冷却结晶(填操作名称)、过滤、洗涤干燥.
(3)室温下,将NaOH溶液逐滴加入到浓度均为0.1mol/L的MgCl2和CuCl2混合溶液中,先生成的沉淀是Cu(OH)2.(室温时KSP[Mg(OH)2]=1.8×10-11,KSP[Cu(OH)2]=2.2×10-20)
(4)某学习小组用碘量法测定CuCl2•2H2O样品的纯度(杂质不与发生反应).实验如下:
a.准确称取CuCl2•2H2O样品mg于小烧杯中,加入适量蒸馏水和足量的碘化钾,再滴入适量的稀硫酸,充分反应后,将所得混合液配成250mL待测溶液.(已知:2Cu2++4I-═2CuI+I2)
b.移取25.00mL待测溶液于锥形瓶中,加几滴指示剂,用c mol•L-1Na2S2O3标准液滴定至终点,重复2次,测得消耗标准液体积的平均值为V mL.(已知:I2+2S2O32-═2I-+S4O62-)
①实验中使用的指示剂名称为淀粉,达到滴定终点时的溶液颜色变化为溶液由蓝色变为无色.
②该样品中CuCl2•2H2O 的质量分数为$\frac{{171cV×{{10}^{-3}}×10}}{m}×100%$(用含m、c、V的代数式表示,不用化简).
9.下列离子方程式正确的是( )
| A. | NaHCO3溶液呈碱性的原因:HCO3-+H2O?CO32-+H3O+ | |
| B. | 向明矾溶液中逐滴加入Ba(OH)2溶液至沉淀质量最大:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| C. | 氢氧化铝溶于醋酸溶液:Al(OH)3+3H+═Al3++3H2O | |
| D. | 氯化铝溶液中加入过量氨水Al3++4OH-═AlO2-+2H2O |
19.下列结论正确的是( )
| A. | S(g)+O2(g)═SO2(g)△H1;S(s)+O2(g)═SO2(g)△H2,则△H1<△H2 | |
| B. | C(石墨,s)=C(金刚石,s)△H=+1.9 kJ•mol-1,则金刚石比石墨稳定 | |
| C. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4 kJ•mol-1,则含20 g NaOH的稀溶液与稀醋酸恰好完全反应,放出的热量为28.7 kJ | |
| D. | 2C(s)+O2(g)═2CO(g)△H=-221 kJ•mol-1,则碳的燃烧热等于110.5 kJ•mol-1 |
6.25℃时,某酸性溶液中只含NH4+、Cl-、H+、OH-四种离子,下列说法不正确的是( )
| A. | 可能由pH=2的盐酸与pH=12的氨水等体积混合而成 | |
| B. | 该溶液可能由等物质的量浓度的盐酸和氨水等体积混合而成 | |
| C. | 加入适量氨水,溶液中离子浓度可能为:c (NH4+)>c (Cl-)>c (OH-)>c(H+) | |
| D. | 该溶液中c (NH4+)=c (Cl-)+c (OH-)-c(H+) |
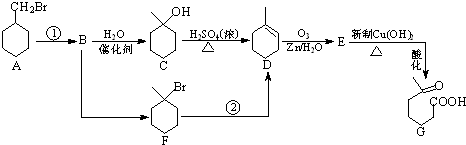
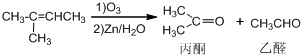
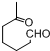 +NaOH+2Cu(OH)2$\stackrel{△}{→}$
+NaOH+2Cu(OH)2$\stackrel{△}{→}$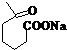 +Cu2O↓+3H2O;
+Cu2O↓+3H2O; 物质D与呋喃(
物质D与呋喃(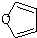 )也可以发生“Diels-Alder反应”,该化学反应方程式为
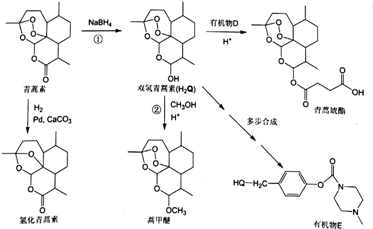
)也可以发生“Diels-Alder反应”,该化学反应方程式为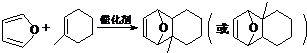 .
.
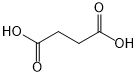 (或
(或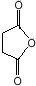 ).
). .
.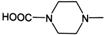 外,还需含苯环的二羟基化合物P,其结构简式为
外,还需含苯环的二羟基化合物P,其结构简式为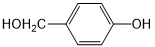 .化合物S是P的同分异构体,其分子结构含有苯环,有4种不同类型的氢,且个数比为3:2:2:1,写出S的一种结构简式
.化合物S是P的同分异构体,其分子结构含有苯环,有4种不同类型的氢,且个数比为3:2:2:1,写出S的一种结构简式 (或
(或 ,其他合理答案亦可).
,其他合理答案亦可).