题目内容
下列说法正确的是( )
| A、金属阳离子只有氧化性 |
| B、金属氧化物一定是碱性氧化物 |
| C、焰色反应是金属元素的一种化学性质 |
| D、22g二氧化碳与标准状况下的11.2L HCl含有相同的分子数 |
考点:焰色反应,阿伏加德罗常数,常见金属元素的单质及其化合物的综合应用
专题:阿伏加德罗常数和阿伏加德罗定律,几种重要的金属及其化合物
分析:A、低价金属阳离子既可以失电子还可以得电子;
B、金属氧化物不一定是碱性氧化物;
C、焰色反应不是化学性质;
D、根据n=
=
计算二氧化碳、HCl物质的量,再由N=nNA判断.
B、金属氧化物不一定是碱性氧化物;
C、焰色反应不是化学性质;
D、根据n=
| m |
| M |
| V |
| Vm |
解答:
解:A、金属原子只能失电子,只有还原性,低价金属阳离子如亚铁离子既可以失电子还可以得电子,既有氧化性又有还原性,故A错误;
B、金属氧化物不一定是碱性氧化物,如过氧化钠,不是碱性氧化物,故B错误;
C、焰色反应不是化学性质,是一种元素的物理性质,故C错误;
D、22g二氧化碳的物质的量=
=0.5mol,标准状况下的11.2L HCl的物质的量=
=0.5mol,二者物质的量相等,由N=nNA可知,二者含有分子数目相等,故D正确.
故选D.
B、金属氧化物不一定是碱性氧化物,如过氧化钠,不是碱性氧化物,故B错误;
C、焰色反应不是化学性质,是一种元素的物理性质,故C错误;
D、22g二氧化碳的物质的量=
| 22g |
| 44g/mol |
| 11.2L |
| 22.4L/mol |
故选D.
点评:本题考查气体摩尔体积和焰色反应以及碱性氧化物,难度不大,注意气体摩尔体积的使用条件及对象.

练习册系列答案
相关题目
下列说法正确的是( )
| A、pH=8的溶液一定显碱性 |
| B、某反应,其他条件不变,升高温度使化学平衡常数(K)增大,则此反应为放热反应 |
| C、相同物质的量浓度的下列溶液中:①NH4Al(SO4)2、②NH4Cl、③CH3COONH4,则c(NH4+)由大到小的顺序是:①>②>③ |
| D、0.1 mol.L-1 的碳酸钠溶液中:c(OH-)=c(H+)-c(HCO3-)+c(H2CO3) |
化学与人类生活、能源开发、资源利用等密切相关.下列说法正确的是( )
| A、塑料奶瓶比玻璃奶瓶更有利于健康,且更加经久耐用 |
| B、“绿色化学”的核心是利用化学原理,解决和治理环境污染问题 |
| C、硅燃烧放出的热量多,且燃烧产物对环境污染程度低,可做“未来石油” |
| D、秸秆的综合利用,如发酵制沼气、生产乙醇等,工艺复杂,还不如一把火烧光还田来得方便 |
关于油脂在人体中的生理功能,下列说法正确的是( )
①油脂在人体内的水解、氧化可释放能量,所以油脂可在人体内提供能量;
②为人体合成其他化合物提供原料;
③保持体温,保护内脏器官.
①油脂在人体内的水解、氧化可释放能量,所以油脂可在人体内提供能量;
②为人体合成其他化合物提供原料;
③保持体温,保护内脏器官.
| A、都正确 | B、只有①② |
| C、只有①③ | D、只有②③ |
表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG=lg
,则下列叙述正确的是( )
| c(H+) |
| c(OH) |
| A、中性溶液的AG=0 |
| B、常温下0.lmol/L氢氧化钠溶液AG=12 |
| C、酸性溶液的AG<0 |
| D、常温下0.lmol/L盐酸溶液的AG=12 |
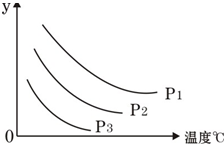
可逆反应L(s)+G(g)?2R(g),由图分析y所表示的量以及反应的能量变化为(图中压强P1>P2>P3( )

| A、G的体积分数,正反应为吸热反应 |
| B、R的体积分数,正反应为吸热反应 |
| C、G的转化率,正反应为放热反应 |
| D、R的分解率,正反应为放热反应 |
合成氨所需的氢气由煤与水发生反应制得,其中一步反应为:CO(g)+H2O(g)?CO2(g)+H2(g);△H<0,要使CO转化率提高,可采用下列措施中的( )
| A、增大水蒸气的浓度 |
| B、增大CO的浓度 |
| C、升高温度 |
| D、增大压强 |
设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、16g O3与 O2混合物中所含氧原子数为NA |
| B、2.3gNa+中含有的电子数为0.1NA |
| C、在常温常压下11.2L二氧化碳所含的分子数目为0.5NA |
| D、相同质量的两块钠分别变成氧化钠和过氧化钠前者失去的电子数多 |